题目内容
实验需要0.1mol/LNaOH溶液950ml,根据溶液配制中情况回答下列问题:
(1)实验中除了托盘天平、烧杯、量筒外还需要的其它仪器有: .
(2)根据计算得知,所需NaOH的质量为 g.
(3)下列操作对所配浓度有何影响(填写字母)偏大的有 ;无影响的有 .
A.称量用了生锈的砝码
B.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中
C.容量瓶未干燥即用来配制溶液
D.往容量瓶转移溶液时,有少量液体溅出
E.定容时仰视刻度线
F.定容后反复摇匀,静置后,液面不到刻度线,再加水至刻度线.
(1)实验中除了托盘天平、烧杯、量筒外还需要的其它仪器有:
(2)根据计算得知,所需NaOH的质量为
(3)下列操作对所配浓度有何影响(填写字母)偏大的有
A.称量用了生锈的砝码
B.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中
C.容量瓶未干燥即用来配制溶液
D.往容量瓶转移溶液时,有少量液体溅出
E.定容时仰视刻度线
F.定容后反复摇匀,静置后,液面不到刻度线,再加水至刻度线.
考点:溶液的配制
专题:实验题
分析:(1)根据配制步骤是计算、称量、溶解、洗涤、定容、摇匀、装瓶来分析需要的仪器;
(2)根据n=cV和m=nM来计算;
(3)根据c=
进行误差分析,如果溶质的物质的量偏大或溶液的体积偏小都使配制溶液浓度偏高,如果溶质的物质的量和溶液的体积都不变则对C无影响,据此分析解答.
(2)根据n=cV和m=nM来计算;
(3)根据c=
| n |
| V |
解答:
解:(1)没有950mL规格容量瓶,所以选用1000mL容量瓶.
操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解.冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以所需仪器有托盘天平、烧杯、玻璃棒、1000mL容量瓶、胶头滴管.
根据提供的仪器可知,还需仪器有玻璃棒、1000ml容量瓶、胶头滴管.
故答案为:玻璃棒、1000ml容量瓶、胶头滴管.
(2)需氢氧化钠的质量为m=1L×0.1mol?L-1×40g/mol=4.0g.
故答案为:4.0g.
(3)A.生锈后砝码质量增重,由于m物=m砝+m游,故称量出的药品的质量偏高,故浓度偏大;
B.NaOH在烧杯中溶解时放热,未冷却就立即转移到容量瓶中,则冷却后溶液体积偏小,浓度偏大;
C.最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响;
D.往容量瓶转移时,有少量液体溅出,移入容量瓶中的氢氧化钠的质量减小,所配溶液浓度偏低;
E.定容时仰视刻度线,导致溶液体积增大,所配溶液浓度偏低;
F.摇匀后液面下降,一部分溶液留在瓶塞与瓶口之间,再加蒸馏水至刻度线,导致溶液体积偏大,所以溶液浓度偏小.
故答案为:AB;C.
操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解.冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以所需仪器有托盘天平、烧杯、玻璃棒、1000mL容量瓶、胶头滴管.
根据提供的仪器可知,还需仪器有玻璃棒、1000ml容量瓶、胶头滴管.
故答案为:玻璃棒、1000ml容量瓶、胶头滴管.
(2)需氢氧化钠的质量为m=1L×0.1mol?L-1×40g/mol=4.0g.
故答案为:4.0g.
(3)A.生锈后砝码质量增重,由于m物=m砝+m游,故称量出的药品的质量偏高,故浓度偏大;
B.NaOH在烧杯中溶解时放热,未冷却就立即转移到容量瓶中,则冷却后溶液体积偏小,浓度偏大;
C.最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响;
D.往容量瓶转移时,有少量液体溅出,移入容量瓶中的氢氧化钠的质量减小,所配溶液浓度偏低;
E.定容时仰视刻度线,导致溶液体积增大,所配溶液浓度偏低;
F.摇匀后液面下降,一部分溶液留在瓶塞与瓶口之间,再加蒸馏水至刻度线,导致溶液体积偏大,所以溶液浓度偏小.
故答案为:AB;C.
点评:本题考查了一定物质的量浓度溶液的配制过程中的计算和仪器的选择,注意从c=
理解误差分析的原理.
| n |
| V |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列关于稀有气体的叙述不正确的是( )
| A、各原子轨道电子均已填满 |
| B、其原子与同周期ⅠA、ⅡA族阳离子具有相同的核外电子排布 |
| C、化学性质非常不活泼 |
| D、同周期中第一电离能最大 |
下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
| A、0.1mol/L NaHCO3溶液中:c(H+)+c(Na+)=c(OH-)+c(HCO3-)+c(CO32-) |
| B、一定量(NH4)2SO4与NH3?H2O混合所得的酸性溶液中:c(NH4+)=2c(SO42-) |
| C、将0.2mol/L CH3COOH溶液和0.1mol/L NaOH溶液等体积混合,则反应后的混合液中:c(OH-)+c(CH3COO-)=c(H+)+c(Na+) |
| D、物质的量浓度相等的①NH4HSO4溶液、②NH4HCO3溶液、③NH4Cl溶液中,c(NH4+)的大小关系:①>②>③ |
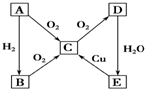 在通常状况下,A为固态单质.根据图转化关系,回答:
在通常状况下,A为固态单质.根据图转化关系,回答: 按图装置进行实验,并回答下列问题:
按图装置进行实验,并回答下列问题: