题目内容
14.对于反应N2+3H2?2NH3,欲使正反应速率增大,可采取( )| A. | 减小NH3的浓度 | B. | 降低反应体系的温度 | ||
| C. | 降低压强 | D. | 缩小容器体积 |
分析 恒温条件下,达到平衡后,欲使正反应速率增大,可以通过增大反应物浓度、升高温度、增大压强、加入催化剂等方法实现,以此解答.
解答 解:A.减小NH3的浓度,反应速率减小,故A错误;
B.降低反应体系的温度,活化分子百分数减小,反应速率减小,故B错误;
C.降低压强,浓度减小,反应速率减小,故C错误;
D.缩小容器容积,增大压强,增大单位体积内活化分子个数,正反应速率增大,故D正确.
故选D.
点评 本题考查化学反应速率影响因素,为高频考点,侧重考查学生分析判断能力,注意把握外界条件对反应速率的影响,难度不大.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
5.对于化学反应方向的确定,下列说法正确的是( )
| A. | 固体的溶解过程与焓变有关 | |
| B. | 温度、压强一定时,放热的熵增加反应不一定能自发进行 | |
| C. | 反应焓变是决定反应能否自发进行的唯一因素 | |
| D. | 在温度、压强一定的条件下,焓因素和熵因素共同决定一个化学反应的方向 |
9.目前已发现和人工合成的有机物有3000多万种,其品种如此众多是由于( )
| A. | 它们都含有碳、而且碳原子有四个价电子,碳原子间以及碳与其他原子间结构多样 | |
| B. | 它们反应很复杂 | |
| C. | 制取它们的方法很多 | |
| D. | 它们都是非电解质 |
19.下列实验操作或装置(略去部分加持仪器)正确的是( )
| A. | 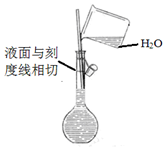 配制溶液 | B. | 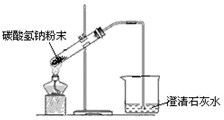 碳酸氢钠受热分解 | ||
| C. | 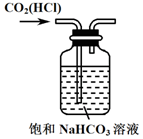 除去CO2中的HCl | D. | 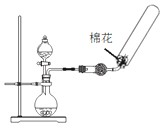 制备收集干燥氨气 |
6.如图是以石油为原料的部分转化流程,则下列说法正确的是( )
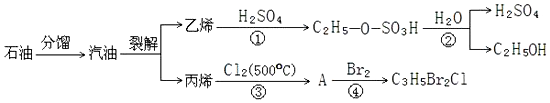

| A. | 石油分馏和裂解均属于化学变化 | |
| B. | 反应①②表明硫酸可用于乙烯水化法制乙醇的催化剂 | |
| C. | 反应①与反应④均属于加成反应 | |
| D. | 反应③的原子利用率为100% |
3.药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:
 ,说法正确的是( )
,说法正确的是( )
 ,说法正确的是( )
,说法正确的是( )| A. | 贝诺酯分子中有三种含氧官能团 | |
| B. | 可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚 | |
| C. | 乙酰水杨酸和对乙酰氨基酚均能与NaHCO3溶液反应 | |
| D. | 贝诺酯与足量NaOH溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠 |
4.一定温度下,在三个体积均为2.0L的恒容密闭容器中发生反应:PCl5(g)?PCl3(g)+Cl2(g),相关信息如表所示:
下列说法正确的是( )
| 编号 | 温度(℃) | 起始物质的量 (mol) | 平衡物质的量 (mol) | 达到平衡所需时间 (s) | |
| PCl5(g) | PCl3(g) | Cl2(g) | |||
| Ⅰ | 320 | 0.40 | 0.10 | 0.10 | 2 |
| Ⅱ | 320 | 0.80 | t1 | ||
| Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t2 |
| A. | 平衡常数K:容器Ⅱ>容器Ⅲ | |
| B. | 反应到达平衡时,容器Ⅱ中PCl5的转化率小于25% | |
| C. | 反应到达平衡时,容器I中的平均速率为v(PCl5)=0.05mol•L-1•s-1 | |
| D. | 起始时向容器Ⅲ中充入0.30molPCl5、0.45molPCl3和0.10molCl2,则反应将向逆反应方向进行 |