题目内容
16.按要求写出化学式或方程式(1)氢氧化钡溶液和硫酸铜溶液反应的离子方程式Ba2++2OH-+Cu2++SO42-=Cu(OH)2↓+BaSO4↓.
(2)除去CO2中混有HCl气体,选用试剂为饱和碳酸氢钠溶液,对应的离子方程式H++HCO3-═H2O+CO2↑.
(3)NaHSO4与Ba(OH)2以物质的量之比1:1混合的离子方程式H++SO42-+Ba2++OH-=BaSO4↓+H2O.
(4)CO2+2OH-=CO32-+H2O对应的一个化学方程式CO2+2NaOH=Na2CO3+H2O.
分析 (1)氢氧化钡溶液和硫酸铜溶液的反应,生成硫酸钡和氢氧化铜;
(2)HCl能和碳酸氢钠反应,而二氧化碳和碳酸氢钠不反应;
(3)NaHSO4与Ba(OH)2以物质的量之比1:1混合,发生NaHSO4+Ba(OH)2=BaSO4↓+NaOH+H2O;
(4)该离子方程式表示二氧化碳与强碱反应生成可溶性的碳酸盐.
解答 解:(1)氢氧化钡溶液和硫酸铜溶液的反应的离子反应为Ba2++2OH-+Cu2++SO42-=Cu(OH)2↓+BaSO4↓,
故答案为:Ba2++2OH-+Cu2++SO42-=Cu(OH)2↓+BaSO4↓;
(2)HCl能和碳酸氢钠反应,而二氧化碳和碳酸氢钠不反应,故可以饱和碳酸氢钠溶液除去二氧化碳中的HCl气体,反应为:H++HCO3-═H2O+CO2↑,故答案为:H++HCO3-═H2O+CO2↑;
(3)NaHSO4与Ba(OH)2以物质的量之比1:1混合,发生NaHSO4+Ba(OH)2=BaSO4↓+NaOH+H2O,离子反应为H++SO42-+Ba2++OH-=BaSO4↓+H2O,
故答案为:H++SO42-+Ba2++OH-=BaSO4↓+H2O;
(4)该离子方程式表示二氧化碳与强碱反应生成可溶性的碳酸盐,如CO2+2NaOH=Na2CO3+H2O,故答案为:CO2+2NaOH=Na2CO3+H2O.
点评 本题考查化学方程式、离子方程式书写方法和注意问题,反应的实质和产物判断是解题关键,题目较简单.

练习册系列答案
相关题目
6. Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于表:
Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于表:
回答下列问题:
(1)Mn元素价电子层的电子排布式为3d54s2,比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难.对此,你的解释是由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态(或Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态);
(2)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是具有孤对电子;
②六氰合亚铁离子(Fe(CN)64-)中的配体CN-中C原子的杂化轨道类型是sp,写出一种与CN-互为等电子体的单质分子的路易斯结构式:N≡N:;
(3)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华.易溶于水,也易溶于乙醚、丙酮
等有机溶剂.据此判断三氯化铁晶体为分子晶体;
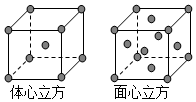
(4)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示.面心立方晶胞和体心立方晶胞中实际
含有的Fe原子个数之比为2:1.
 Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于表:
Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于表:| 元 素 | Mn | Fe | |
| 电离能 /kJ•mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
(1)Mn元素价电子层的电子排布式为3d54s2,比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难.对此,你的解释是由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态(或Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态);
(2)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是具有孤对电子;
②六氰合亚铁离子(Fe(CN)64-)中的配体CN-中C原子的杂化轨道类型是sp,写出一种与CN-互为等电子体的单质分子的路易斯结构式:N≡N:;
(3)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华.易溶于水,也易溶于乙醚、丙酮
等有机溶剂.据此判断三氯化铁晶体为分子晶体;
(4)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示.面心立方晶胞和体心立方晶胞中实际
含有的Fe原子个数之比为2:1.
7.下列对有机化合物的分类结果正确的是( )
| A. | 乙烯、苯、环己烷都属于脂肪烃 | B. | 苯、环戊烷、环己烷同属于芳香烃 | ||
| C. | 乙烯、乙炔同属于烯烃 | D. |  、 、 、 、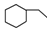 同属于环烷烃 同属于环烷烃 |
4.下列有关气体摩尔体积的说法中正确的是( )
| A. | 在常温常压下,0.5 mol任何气体的体积都必定是11.2 L | |
| B. | 在标准状况下,1 mol任何物质的体积都约是22.4 L | |
| C. | 常温常压下,1 mol任何气体的体积都约是22.4 L | |
| D. | 在标准状况下,0.5 mol CO2所占有的体积约是11.2 L |
1.对于胃溃疡较重的病人,不适合使用的抑酸剂是( )
| A. | Mg(OH)2 | B. | Al(OH)3 | C. | NaHCO3 | D. | MgCO3 |
8.下列说法正确的是( )
| A. | 增大压强,活化分子数增加,化学反应速率一定增大 | |
| B. | 升高温度,活化分子百分数增加,化学反应速率一定增大 | |
| C. | 加入反应物,使活化分子百分数增加,化学反应速率增大 | |
| D. | 使用催化剂,降低了反应的活化能、反应速率加快,但是活化分子百分数不变 |
5.胃舒平是氢氧化铝胶囊,常用来治疗胃酸(盐酸)过多.其原因是两者存在如下反应:Al(OH)3+3HCl═AlCl3+3H2O,问上述反应属于哪一基本反应类型?( )
| A. | 化合反应 | B. | 分解反应 | C. | 复分解反应 | D. | 置换反应 |
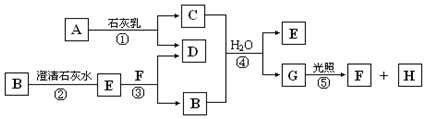 图中A~H均为中学化学中常见的物质,A、B、H是气体,它们之间有如图转化关系(反应中生成的水已略去).
图中A~H均为中学化学中常见的物质,A、B、H是气体,它们之间有如图转化关系(反应中生成的水已略去).