题目内容
16.下列实验能获得成功的是( )| A. | 用酸性高锰酸钾溶液鉴别乙烷和乙烯 | |
| B. | 用分液漏斗分离乙醛和水 | |
| C. | 用苯、溴水和铁粉混合制取溴苯 | |
| D. | 用紫色石蕊溶液检验苯酚弱酸性 |
分析 A.乙烯能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,乙烷性质较稳定,和酸性高锰酸钾溶液不反应;
B.互不相溶的液体采用分液方法分离,互溶的液体采用蒸馏的方法分离;
C.苯和溴水不反应,和液溴在溴化铁作催化剂条件下发生取代反应;
D.苯酚酸性很弱,不能使石蕊溶液变色.
解答 解:A.乙烯能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,乙烷性质较稳定,和酸性高锰酸钾溶液不反应,所以可以用酸性高锰酸钾溶液鉴别乙烷和乙烯,故A正确;
B.互不相溶的液体采用分液方法分离,互溶的液体采用蒸馏的方法分离,乙醛和水互溶,应该采用蒸馏方法分离,故B错误;
C.苯和溴水不反应,和液溴在溴化铁作催化剂条件下发生取代反应,所以该实验不能实现实验目的,故C错误;
D.苯酚俗称石炭酸,酸性很弱,不能使石蕊溶液变色,故D错误;
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及物质鉴别、物质分离和提纯、物质反应条件等知识点,明确实验原理及物质性质是解本题关键,侧重考查学生实验操作及实验评价能力,注意基础知识的总结和归纳.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.室温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | 加入Al能放出H2的溶液中:NH4+,SO42-,Br-,NO3- | |
| B. | 通入过量SO2气体的溶液中:Fe3+、NO3-、Ba2+、H+ | |
| C. | 无色强酸性溶液中:Na+、Cl-、SO42-、Cu2+ | |
| D. | c(I-)=0.1 mol•L-1的溶液中:Na+、Fe2+、Cl-、SO42- |
7.下列递变情况中,不正确的是( )
| A. | Na、Mg、Al原子的最外层电子数依次增多 | |
| B. | Si、P、S元素的最高正价依次升高 | |
| C. | C、N、O的原子半径依次增大 | |
| D. | Li、Na、K的金属性依次增强 |
11.浓硫酸与木炭粉在加热条件下反应.已知酸性KMnO4溶液可以吸收SO2,试用下图所示各装置设计一个实验,验证上述反应所产生的各种产物.
(1)写出木炭与浓硫酸反应的化学方程式C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.标准状况下,若生成6.72L的气体,则转移电子的物质的量为0.4mol.这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号):
④→②→①→③.
(2)实验时可观察到:装置①中A瓶的溶液褪色,C瓶的溶液不褪色.B瓶溶液的作用是将多余的SO2全部氧化吸收,C瓶溶液的作用是确证产物中SO2已被B瓶溶液全部氧化.
(3)装置②中所加的固体药品是无水CuSO4,可确证的产物是水蒸气,确定装置②在整套装置中位置的理由是由于产物气流通过①、③时会带出水蒸气,所以②必须在①、③之前.
(4)盛放浓硫酸的试剂瓶标签上应印有下列警示标记中的D
| 编号 | ① | ② | ③ | ④ |
| 装置 | 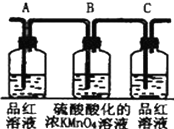 | 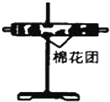 |  |  |
④→②→①→③.
(2)实验时可观察到:装置①中A瓶的溶液褪色,C瓶的溶液不褪色.B瓶溶液的作用是将多余的SO2全部氧化吸收,C瓶溶液的作用是确证产物中SO2已被B瓶溶液全部氧化.
(3)装置②中所加的固体药品是无水CuSO4,可确证的产物是水蒸气,确定装置②在整套装置中位置的理由是由于产物气流通过①、③时会带出水蒸气,所以②必须在①、③之前.
(4)盛放浓硫酸的试剂瓶标签上应印有下列警示标记中的D

8.下列有机化合物命名正确的是( )
| A. | 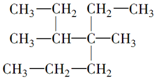 4-甲基-4,5-二乙基乙烷 4-甲基-4,5-二乙基乙烷 | B. | 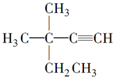 3,3-二甲基-1-戊炔 3,3-二甲基-1-戊炔 | ||
| C. | 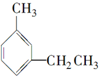 3-甲基乙基苯 3-甲基乙基苯 | D. |  3-甲基-1,3-丁二烯 3-甲基-1,3-丁二烯 |
6.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,且不会造成二次污染.已知高铁酸盐在低温碱性环境中稳定,易溶于水,难溶于无水乙醇等有机溶剂.
常见高铁酸钾的制备方法如下:
(1)干法制备反应中氧化剂和还原剂的物质的量之比为:3:1.
(2)某湿法制备高铁酸钾的基本流程及步骤如下:
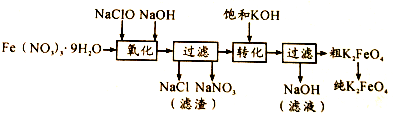
①控制反应温度为25℃,搅拌1.5h,经氧化等过程溶液变为紫红色,该反应的离子方程式为3ClO-+2Fe3++10OH-═2FeO42-+3Cl-+5H2O.
②在紫红色溶液中加入饱和KOH溶液,析出紫黑色晶体,过滤,得到K2FeO4粗产品.沉淀过程中加入饱和KOH溶液得到晶体的原因是该温度下高铁酸钾的溶解度比高铁酸钠的溶解度小.
③K2FeO4粗产品含有Fe(OH)3、KCl等杂质,用重结晶方法进行分离提纯.其提纯步骤为:将一定量的K2FeO4粗产品溶于冷的3mol/LKOH溶液中,过滤,将滤液置于冰水浴中,向滤液中加入饱和KOH溶液,搅拌、静置、过滤,用乙醇洗涤2~3次,在真空干燥箱中干燥.
④若以FeCl3 代替Fe(NO3)3作铁源,K2FeO4的产率和纯度都会降低.一个原因是在反应温度和强碱环境下NaCl的溶解度比NaNO3大,使得NaCl结晶去除率较低;另一个原因是Cl-被FeO42-氧化,消耗产品使产率降低.
(3)工业上还可用通过电解浓NaOH溶液制备Na2FeO4,其工作原理如下图所示:阳极的电极反应为Fe-6e-+8OH-=FeO42-+4H2O;其中可循环使用的物质的电子式是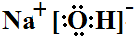 .
.
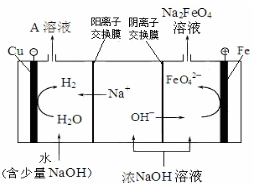
(4)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38、Ksp[Cu(OH)2]=2.2×10-20,向该温度下含有Fe3+、Cu2+浓度均为0.01mol/L的溶液中,滴加浓NaOH溶液,当溶液pH=10时,溶液中c(Cu2+):c(Fe3+)=5.5×1013:1.
常见高铁酸钾的制备方法如下:
| 制备方法 | 具体内容 |
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸钾和KNO2等产物 |
| 湿法 | 强碱性介质中,Fe(NO3)3与KClO反应生成紫红色高铁酸钾溶液 |
| 电解法 | 电解浓NaOH溶液制备Na2FeO4 |
(2)某湿法制备高铁酸钾的基本流程及步骤如下:

①控制反应温度为25℃,搅拌1.5h,经氧化等过程溶液变为紫红色,该反应的离子方程式为3ClO-+2Fe3++10OH-═2FeO42-+3Cl-+5H2O.
②在紫红色溶液中加入饱和KOH溶液,析出紫黑色晶体,过滤,得到K2FeO4粗产品.沉淀过程中加入饱和KOH溶液得到晶体的原因是该温度下高铁酸钾的溶解度比高铁酸钠的溶解度小.
③K2FeO4粗产品含有Fe(OH)3、KCl等杂质,用重结晶方法进行分离提纯.其提纯步骤为:将一定量的K2FeO4粗产品溶于冷的3mol/LKOH溶液中,过滤,将滤液置于冰水浴中,向滤液中加入饱和KOH溶液,搅拌、静置、过滤,用乙醇洗涤2~3次,在真空干燥箱中干燥.
④若以FeCl3 代替Fe(NO3)3作铁源,K2FeO4的产率和纯度都会降低.一个原因是在反应温度和强碱环境下NaCl的溶解度比NaNO3大,使得NaCl结晶去除率较低;另一个原因是Cl-被FeO42-氧化,消耗产品使产率降低.
(3)工业上还可用通过电解浓NaOH溶液制备Na2FeO4,其工作原理如下图所示:阳极的电极反应为Fe-6e-+8OH-=FeO42-+4H2O;其中可循环使用的物质的电子式是
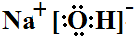 .
.
(4)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38、Ksp[Cu(OH)2]=2.2×10-20,向该温度下含有Fe3+、Cu2+浓度均为0.01mol/L的溶液中,滴加浓NaOH溶液,当溶液pH=10时,溶液中c(Cu2+):c(Fe3+)=5.5×1013:1.
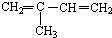 与Br2按物质的量之比1:1发生1,4加成反应的化学方程式CH2=C(CH3)CH=CH2+Br2→CH2BrC(CH3)=CHCH2Br.
与Br2按物质的量之比1:1发生1,4加成反应的化学方程式CH2=C(CH3)CH=CH2+Br2→CH2BrC(CH3)=CHCH2Br. .
. CH3COOC2H5+H2O
CH3COOC2H5+H2O ;
;
 ,OPA分子中最多有16个原子共平面.
,OPA分子中最多有16个原子共平面.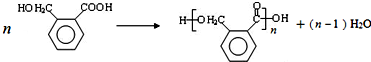 (不必注明反应条件),该反应的类型为缩聚反应.
(不必注明反应条件),该反应的类型为缩聚反应.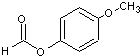 (写出其结构简式).
(写出其结构简式).