题目内容
16.某温度下,容积一定的密闭容器中进行可逆反应:X(g)+Y(g)?2Z(g)+W(s);△H<0,下列叙述正确的是( )| A. | 加入少量W,υ(逆)增大 | B. | 压强不变时,反应达到平衡状态 | ||
| C. | 升高温度,υ(逆)、υ(正)都增大 | D. | 平衡后加入X,方程式中的△H增大 |
分析 对于X(g)+Y(g)?2Z(g)+W(s);△H<0,W为固体,固体不影响化学平衡移动,反应前后气体的体积相等,升高温度,正逆反应都增大,反应热与某一反应物的量无关,以此解答该题.
解答 解:A.W在反应中是固体,固体量的增减不会引起化学反应速率的改变和化学平衡的移动,故A错误;
B.反应前后气体的体积相等,无论是否达到平衡状态,气体的压强都不变,故B错误;
C.升高温度,活化分子的百分数增大,则正逆反应速率都增大,故C正确;
D.热化学方程式中反应热△H与物质的化学计量数有关,物质的化学计量数不变,热化学方程式中反应热不变,与参加反应的物质的物质的量无关,故D错误.
故选C.
点评 本题考查化学平衡的影响因素,为高考常见题型和高频考点,侧重考查学生的分析能力,本题注意反应的特征以及相关概念的连接,难度不大.

练习册系列答案
相关题目
6.设NA为阿伏加徳罗常数值.下列有关叙述正确的是( )
| A. | 2 molSO2与3 molO2反应生成的SO3分子数为2NA | |
| B. | 30 g乙酸和葡萄糖混合物中的氢原子数为2NA | |
| C. | 常温下pH=12的NaOH溶液中,水电离出的氢离子数为10-12NA | |
| D. | 标准状况下,2.24 L C2H6含有的共价键数为0.6NA |
7.下列说法正确的是( )
| A. | 葡萄糖、蔗糖均可发生银镜反应 | |
| B. | 硫酸铵和乙酸铅均能使蛋白质发生变性 | |
| C. | 乙炔和乙醛均可作为合成聚合物的单体 | |
| D. | 淀粉和油脂都是能够发生水解反应的高分子化合物 |
4.某化合物的化学式为NH5,其电子式为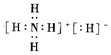 下列有关说法正确的是( )
下列有关说法正确的是( )
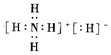 下列有关说法正确的是( )
下列有关说法正确的是( )| A. | 该化合物中氢元素的化合价均为+1价 | |
| B. | 该化合物中只有N原子最外层达到稀有气体的稳定结构 | |
| C. | 该化合物中含有$\stackrel{-1}{H}$与$\stackrel{+1}{H}$,二者互为同位素 | |
| D. | 该化合物中既含有共价键,又含有离子键 |
11.下列关于有机化合物的说法正确的是( )
| A. | 石油裂解和蛋白质水解都是由高分子化合物生成小分子物质的过程 | |
| B. | 乙烯分别使溴水和酸性KMnO4溶液褪色,反应原理相同 | |
| C. | C6H14有5种同分异构体 | |
| D. | CH4和Cl2按体积比1:3混合可制得纯净的CHCl3 |
1.下列关于有机物的叙述正确的是( )
| A. | 聚乙烯塑料中含有大量碳碳双键,容易老化 | |
| B. | 苯、油脂均不能使酸性KMnO4溶液褪色 | |
| C. | 甲苯苯环上的一个氢原子被一C3H6Cl取代,形成的同分异构体有9种 | |
| D. | CH2═CHCH2OH能发生加成反应、取代反应、氧化反应 |
8. 常温下,将除去表面氧化膜的A1、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示.反应过程中有红棕色气体产生.下列说法错误的是( )
常温下,将除去表面氧化膜的A1、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示.反应过程中有红棕色气体产生.下列说法错误的是( )
 常温下,将除去表面氧化膜的A1、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示.反应过程中有红棕色气体产生.下列说法错误的是( )
常温下,将除去表面氧化膜的A1、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示.反应过程中有红棕色气体产生.下列说法错误的是( )| A. | t1时刻前,A1片的电极反应为:2A1-6e-+3H2O═A12O3+6H+ | |
| B. | t1时,因A1在浓硝酸中钝化,氧化膜阻碍了A1继续反应 | |
| C. | t1之后,负极Cu失电子,电流方向发生改变 | |
| D. | 烧杯中发生的离子反应为:2NO2+2OH-═2NO3-+H2O |
4.醋酸在水中电离方程式可表示为:CH3COOH?CH3COO-+H+△H>0,下列操作能使H+浓度增大的是( )
| A. | 加入少量NaOH固体 | B. | 加热升温10℃ | ||
| C. | 加入锌粉 | D. | 加入固体CH3COONa |
5.下列实验操作或装置正确的是( )
| A. | 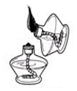 点燃酒精灯 | B. |  往试管中加入锌粒 | ||
| C. | 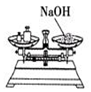 称量氢氧化钠 | D. |  收集氧气 |