题目内容
19.A元素原子M电子层有6个电子,B元素与A元素原子具有相同电子层数,B元素的原子最外层上只有1个电子.(1)画出B元素的原子结构示意图:
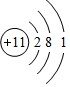 .
.(2)A、B两元素形成的化合物的名称是硫化钠,该化合物在无色火焰上灼烧时,火焰呈黄色.
分析 A元素原子M电子层有6个电子,则K、L层排满电子,所以A元素核外电子数=2+8+6=16,为S元素;
B元素与A元素原子具有相同电子层数,说明位于同一周期,B元素的原子最外层上只有1个电子,则B元素原子核外电子数=2+8+1=11,为Na元素;
(1)B为Na元素,原子核内有11个电子、核外有11个电子、3个电子层;
(2)A、B元素形成的化合物是硫化钠,钠元素焰色反应呈黄色.
解答 解:A元素原子M电子层有6个电子,则K、L层排满电子,所以A元素核外电子数=2+8+6=16,为S元素;
B元素与A元素原子具有相同电子层数,说明位于同一周期,B元素的原子最外层上只有1个电子,则B元素原子核外电子数=2+8+1=11,为Na元素;
(1)B为Na元素,原子核内有11个电子、核外有11个电子、3个电子层,则Na原子结构示意图为 ,故答案为:
,故答案为: ;
;
(2)A、B元素形成的化合物是Na2S,名称是硫化钠,钠元素焰色反应呈黄色,所以硫化钠焰色反应呈黄色,故答案为:硫化钠;黄.
点评 本题考查位置结构性质相互关系及应用,明确原子结构、元素周期表结构是解本题关键,注意:焰色反应是元素的性质,不是物质的性质,且焰色反应是物理变化.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
10. Bodensteins 研究了反应+I2(g)?H2(g)+I2(g)△H=+11kL•mol-1在716 K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
Bodensteins 研究了反应+I2(g)?H2(g)+I2(g)△H=+11kL•mol-1在716 K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
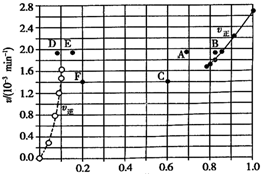
由上述实验数据计箅得到v正~x( HI)和v逆~x( H2)的 关系可用如图表示.当改变条件,次再达到平衡时,下列有关叙述不正确的是( )
 Bodensteins 研究了反应+I2(g)?H2(g)+I2(g)△H=+11kL•mol-1在716 K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
Bodensteins 研究了反应+I2(g)?H2(g)+I2(g)△H=+11kL•mol-1在716 K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:| l/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
| A. | 若升高温度到某一温度,则再次达到平衡时,相应点 可能分別是A、E | |
| B. | 若再次充人a molHI,则达到平衡时,相应点的播坐 标值不变,纵坐标值增大 | |
| C. | 若改变的条件是增大压强,则再次达到平衡时,相应 点与改变条件前相间 | |
| D. | 若改变的条件是使用催化剂.则再次达到平衡时,相 应点与改变条件前不间. |
4.分子式为C4H8的烯烃共有(要考虑顺反异构体)几种结构( )
| A. | 5种 | B. | 4种 | C. | 3种 | D. | 2种 |
11.为有效除去粗盐中Ca2+、Mg2+、SO42-,加入试剂的合理顺序为( )
| A. | 先加NaOH,后加Na2CO3,再加BaCl2 | B. | 先加NaOH,后加BaCl2,再加Na2CO3 | ||
| C. | 先加Na2CO3,后加BaCl2,再加NaOH | D. | 以上答案皆可 |
9.以下是对某水溶液进行离子检验的方法和结论,其中不正确的是( )
| A. | 先加入BaCl2溶液,产生了白色沉淀,再加入足量的HCl溶液,沉淀不溶解,溶液中一定含有大量SO${\;}_{4}^{2-}$ | |
| B. | 加入足量的CaCl2溶液,产生了白色沉淀,加入盐酸可以产生无色且能使澄清石灰水变浑浊的气体,则该溶液不一定含有大量的CO${\;}_{3}^{2-}$ | |
| C. | 加入足量浓 NaOH溶液加热,产生了带有强烈刺激性气味的能使湿润的红色石蕊试纸变蓝的气体,溶液中一定含有大量的NH${\;}_{4}^{+}$ | |
| D. | 先加适量的硝酸将溶液酸化,再加AgNO3溶液,产生了白色沉淀.溶液中一定含有大量的Cl- |
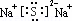
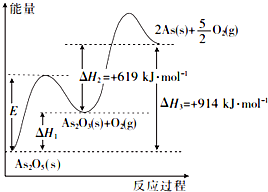 砷的常见酸性氧化物有As2O3和As2O5,根据图中信息回答下列问题:
砷的常见酸性氧化物有As2O3和As2O5,根据图中信息回答下列问题: