题目内容
6.把a、b、c、d四块金属浸入稀硫酸中,用导线两两相连组成原电池,若a、b 相连时,a为负极;c、d相连时,电流由d到c;a、c相连时,c极上产生大量气泡;b、d相连时,d极板溶解,则四种金属的活动性顺序为( )| A. | a>b>c>d | B. | a>c>d>b | C. | c>a>b>d | D. | b>d>c>a |
分析 形成原电池时,活泼金属做负极,根据电极反应现象首先判断电池的正负极,再判断金属的活泼性强弱,电子从负极沿导线流向正极,据此分析解答.
解答 解:形成原电池时,活泼金属做负极,若a、b相连时,a为负极,则金属活动性a>b;c、d相连时,电流由d到c,所以d为正极,金属活泼性为:c>d;a、c相连时,c极上产生大量气泡,说明在c极上产生氢气,c极上发生还原反应,c极为正极,则活动性a>c;b、d相连时,d极板溶解,则金属活动性d>b,所以四种金属的活动性顺序为a>c>d>b,故选B.
点评 本题考查金属的活动性的顺序强弱比较,题目难度不大,本题考查角度为形成原电池反应,注意活泼金属做负极.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.关于反应Zn+2HNO3+NH4NO3═N2↑+3H2O+Zn(NO3)2,下列判断正确的是( )
| A. | 生成1 mol N2,电子转移总数为3NA | B. | 生成1 mol N2,电子转移总数为5NA | ||
| C. | 溶解1 mol Zn,电子转移总数为2NA | D. | 溶解1 mol Zn,电子转移总数为4NA |
17.有机物(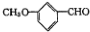 )有多种同分异构体,其中能与NaHCO3溶液反应且属于芳香族化合物的共有( )
)有多种同分异构体,其中能与NaHCO3溶液反应且属于芳香族化合物的共有( )
 )有多种同分异构体,其中能与NaHCO3溶液反应且属于芳香族化合物的共有( )
)有多种同分异构体,其中能与NaHCO3溶液反应且属于芳香族化合物的共有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
14.在氢氧化钠溶液中加入一定量的稀盐酸后,下列实验能证明两者恰好完全中和的是( )
| A. | 滴入适量AgNO3溶液和稀硝酸,观察到有白色沉淀 | |
| B. | 滴入适量FeCl3溶液,溶液变黄,但无沉淀生成 | |
| C. | 测得反应后溶液中Na+与Cl-的个数比为1:1 | |
| D. | 滴入几滴酚酞试液,酚酞试液不变色 |
1.苹果酸是一种常见的有机酸,其结构简式为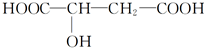 .苹果酸可能发生的反应是( )
.苹果酸可能发生的反应是( )
①与NaOH溶液反应
②与石蕊试液作用变红
③与金属钠反应放出气体
④一定条件下与乙酸酯化
⑤一定条件下与乙醇酯化.
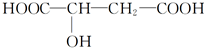 .苹果酸可能发生的反应是( )
.苹果酸可能发生的反应是( )①与NaOH溶液反应
②与石蕊试液作用变红
③与金属钠反应放出气体
④一定条件下与乙酸酯化
⑤一定条件下与乙醇酯化.
| A. | 只有①②③ | B. | 只有②③④ | C. | 只有①②⑤ | D. | ①②③④⑤ |
18.为了配制NH4+浓度与 NO3-的浓度比为1:1的溶液,可在NH4NO3 溶液中加入①适量的HNO3 ②适量的NaNO3 ③适量的氨水④适量的NaOH,正确的是( )
| A. | ①② | B. | ③ | C. | ③④ | D. | ④ |
15.下列措施对增大化学反应速率明显有效的是( )
| A. | Na与水反应时增大水的用量 | |
| B. | Fe与稀硫酸反应制取氢气时,改用浓硫酸 | |
| C. | 在K2SO4与BaCl2两溶液反应时,增大压强 | |
| D. | 将铝片改为铝粉,做铝与氧气反应的实验 |
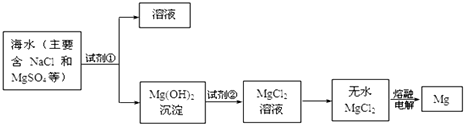
 ,所含化学键的类型离子键和极性共价键;D、E的最高价氧化物对应水化物发生反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O用电子式表示BA3的形成过程3H•+
,所含化学键的类型离子键和极性共价键;D、E的最高价氧化物对应水化物发生反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O用电子式表示BA3的形成过程3H•+ →
→ ,A、C形成的化合物中,C的质量分数最高的化合物的结构式H-O-O-H,C2-的离子结构示意图
,A、C形成的化合物中,C的质量分数最高的化合物的结构式H-O-O-H,C2-的离子结构示意图 ,A有多种同位素,其中一种同位素原子核内有两个中子,这种同位素原子的表示方法31H或T
,A有多种同位素,其中一种同位素原子核内有两个中子,这种同位素原子的表示方法31H或T