题目内容
若在1L蒸馏水中加入1滴(约0.05mL)0.1mol?L-1的NaCl溶液,搅拌均匀后再滴入1滴0.1mol?L-1 AgNO3溶液是否会产生沉淀(已知AgCl的Ksp=1.8×10-10)( )
| A、否 | B、是 |
| C、可能是 | D、以上都不正确 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:氯化银的溶解平衡为:AgCl(s)?Ag++Cl-,Ksp=c(Ag+).c(Cl-),依据题给的氯离子、银离子的物质的量,混合后体积认为是1L,计算出c(Ag+)、c(Cl-),与Ksp比较判断即可.
解答:
解:解:由AgCl(s)?Ag++Cl-,Ksp=c(Ag+).c(Cl-),混合后溶液体积是1L,n(Cl-)=n(Ag+)=0.1mol/L×5×10-5L=5×10-6mol/L,故c(Ag+)c(Cl-)=5×10-6mol/L×5×10-6mol/L=2.5×10-11mol2?L-2<1.8×10-10mol2?L-2,故无AgCl沉淀析出.
故选A.
故选A.
点评:本题考查了根据难溶电解质溶度积判断沉淀情况,注意混合后溶液的体积的变化,题目难度一般.

练习册系列答案
相关题目
下列分散系最不稳定的是( )
| A、向CuSO4溶液中加入Ba(OH)2溶液得到的分散系 |
| B、向水中加入食盐得到的分散系 |
| C、向沸水中滴入饱和FeCl3溶液得到的红褐色液体 |
| D、向NaOH溶液中通入CO2得到的无色溶液 |
下列反应的离子方程式书写正确的是( )
| A、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
| B、Cl2和H2O反应:Cl2+H2O═2H++Cl-+ClO- |
| C、盐酸与Na2SiO3溶液:SiO32-+2H+═H2SiO3↓ |
| D、铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ |
下列高聚物必须是由两种不同的单体经加聚反应而生成的是( )
A、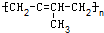 |
B、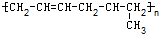 |
C、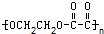 |
D、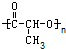 |
下列叙述正确的是( )
| A、可以根据PbI2和AgCl的Ksp的大小比较两者的溶解度 |
| B、常温下,同浓度的Na2S与NaHS溶液相比,NaHS溶液的pH大 |
| C、等物质的量浓度的CH3COONH4溶液和NH4HSO4溶液,前者的c(NH4+)小 |
| D、用惰性电极电解饱和NaCl溶液,若有1.0 mol电子转移,则理论生成1.0 mol NaOH |
对已达平衡的反应2X(g)+Y(g)?4Z(g),改变以下哪种条件能使速率变化如图所示( )


| A、增大Z的浓度 |
| B、减小X的浓度 |
| C、增大压强 |
| D、减小压强 |



 一定条件下聚合生成一种合成纤维:
一定条件下聚合生成一种合成纤维: .
.