题目内容
下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质.气体B与气体C相遇产生大量的白烟,D是日常生活中常见的盐(部分反应物和生成物及溶剂水已略去).

请回答下列问题:
(1)甲元素在周期表中的位置 .
(2)B的电子式为 ;
(3)写出A溶液和丁反应生成D的离子方程式 ;
(4)写出A和E反应的化学方程式 .

请回答下列问题:
(1)甲元素在周期表中的位置
(2)B的电子式为
(3)写出A溶液和丁反应生成D的离子方程式
(4)写出A和E反应的化学方程式
考点:无机物的推断
专题:推断题
分析:乙、丙为单质,在高温高压下催化生成B,且B与C相遇生成大量白烟,可知B为NH3,C为HCl,由转化关系可知丙为H2,乙为N2,E为NH4Cl,则丁为Cl2,D是日常生活中常见的盐,为NaCl,A与E反应可生成氨气,则A应为NaOH,金属甲可与NaOH反应生成H2,则甲为Al,结合对应物质的性质以及题目要求可解答该题.
解答:
解:乙、丙为单质,在高温高压下催化生成B,且B与C相遇生成大量白烟,可知B为NH3,C为HCl,由转化关系可知丙为H2,乙为N2,E为NH4Cl,则丁为Cl2,D是日常生活中常见的盐,为NaCl,A与E反应可生成氨气,则A应为NaOH,金属甲可与NaOH反应生成H2,则甲为Al,
(1)由以上分析可知甲为Al,原子核外有3个电子层,最外层电子数为3,位于周期表第三周期第ⅢA族,故答案为:第三周期第ⅢA族;
(2)B为NH3,为共价化合物,电子式为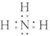 ,故答案为:
,故答案为: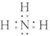 ;
;
(3)氯气在NaOH溶液中发生反应生成氯化钠和次氯酸钠,反应的离子方程式为:2OH-+Cl2=Cl-+ClO-+H2O,故答案为:2OH-+Cl2=Cl-+ClO-+H2O;
(4)NaOH和NH4Cl在加热条件下反应生成氨气,反应的方程式为NaOH+NH4Cl
NH3↑+NaCl+H2O,故答案为:NaOH+NH4Cl
NH3↑+NaCl+H2O.
(1)由以上分析可知甲为Al,原子核外有3个电子层,最外层电子数为3,位于周期表第三周期第ⅢA族,故答案为:第三周期第ⅢA族;
(2)B为NH3,为共价化合物,电子式为
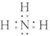 ,故答案为:
,故答案为: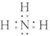 ;
;(3)氯气在NaOH溶液中发生反应生成氯化钠和次氯酸钠,反应的离子方程式为:2OH-+Cl2=Cl-+ClO-+H2O,故答案为:2OH-+Cl2=Cl-+ClO-+H2O;
(4)NaOH和NH4Cl在加热条件下反应生成氨气,反应的方程式为NaOH+NH4Cl
| ||
| ||
点评:本题考查无机物的推断,侧重于分析能力的考查,该题的突破口为物质的颜色,含量以及物质之间的转化关系,答题时注意体会推断思路,题目难度不大.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
NA代表阿伏加德罗常数,下列叙述正确的是( )
| A、50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA |
| B、常温常压下,48 gO2和O3的混合气体中含有的氧原子数为3NA |
| C、在标准状况下,11.2L O2和22.4 L NO混合并充分反应后得到的气体分子数为NA |
| D、常温下5.6克铁投入到足量浓硝酸中反应,转移电子数为0.3NA |
下列物质属于纯净物的是( )
| A、漂白粉 | B、无污染的空气 |
| C、冰水混合物 | D、盐酸 |
温度为25℃时,将0.23g钠投入到100ml水中充分反应后所得溶液的密度为1g/cm3,则该溶液的PH为( )
| A、1 | B、13 | C、12 | D、10 |