题目内容
25℃时,下列关于电解质及其溶液的说法,正确的是( )
| A、BaSO4在饱和Na2SO4溶液中的溶解度与Ksp均比在纯水中的小 |
| B、若将0.01molNaOH溶于1L水,则溶液中由水电离产生的c(H+)=1×10-12mol?L-1 |
| C、10ml0.5mol?L-1CH3COONa溶液与6ml1mol?L-1盐酸混合:c(Cl-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) |
| D、pH=4的HA与pH=10的BOH溶液等体积混合,所得溶液pH=7,则HA、BOH一定为强酸和强碱 |
考点:离子浓度大小的比较,水的电离,难溶电解质的溶解平衡及沉淀转化的本质,酸碱混合时的定性判断及有关ph的计算
专题:
分析:A.难溶物的溶度积与温度有关,温度不变,则硫酸钡的溶度积不变;
B.氢氧化钠电离的氢氧根离子抑制了水的电离,氢氧化钠溶液中的氢离子是水电离的,由于溶液体积不是1L,无法计算氢氧根离子浓度及水电离的氢离子浓度;
C.混合液中溶质为0.005molCH3COOH、0.001molHCl,0.005molNaCl,根据溶质组成及盐的水解判断溶液中离子浓度大小;
D.有可能为弱酸和弱碱反应,如醋酸和一水合氨,反应生成的醋酸铵为中性溶液.
B.氢氧化钠电离的氢氧根离子抑制了水的电离,氢氧化钠溶液中的氢离子是水电离的,由于溶液体积不是1L,无法计算氢氧根离子浓度及水电离的氢离子浓度;
C.混合液中溶质为0.005molCH3COOH、0.001molHCl,0.005molNaCl,根据溶质组成及盐的水解判断溶液中离子浓度大小;
D.有可能为弱酸和弱碱反应,如醋酸和一水合氨,反应生成的醋酸铵为中性溶液.
解答:
解:A.BaSO4在饱和Na2SO4溶液中的溶解度比在纯水中的小,但是与Ksp与温度有关,温度不变,则硫酸钡的溶度积不变,故A错误;
B.0.01mol氢氧化钠溶于1L水中,所带溶液的体积不是1L,氢氧化钠溶液的浓度不是0.01mol/L,无法计算溶液中水电离的氢离子浓度,故B错误;
C.10 mL 0.5 mol?L-1CH3COONa溶液与6 mL 1 mol?L-1盐酸混合反应后,溶液中溶质为0.005molCH3COOH、0.001molHCl,0.005molNaCl,溶液中c(Cl-)<c(Na+),c(OH-)<c(H+),溶液中离子浓度大小为:c(Cl-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-),故C正确;
D.pH=4的HA与pH=10的BOH溶液等体积混合,所得溶液pH=7,则HA、BOH可能为强酸和强碱,有可能为弱酸与弱碱反应,如醋酸与氨水反应生成的醋酸铵溶液为中性,故D错误;
故选C.
B.0.01mol氢氧化钠溶于1L水中,所带溶液的体积不是1L,氢氧化钠溶液的浓度不是0.01mol/L,无法计算溶液中水电离的氢离子浓度,故B错误;
C.10 mL 0.5 mol?L-1CH3COONa溶液与6 mL 1 mol?L-1盐酸混合反应后,溶液中溶质为0.005molCH3COOH、0.001molHCl,0.005molNaCl,溶液中c(Cl-)<c(Na+),c(OH-)<c(H+),溶液中离子浓度大小为:c(Cl-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-),故C正确;
D.pH=4的HA与pH=10的BOH溶液等体积混合,所得溶液pH=7,则HA、BOH可能为强酸和强碱,有可能为弱酸与弱碱反应,如醋酸与氨水反应生成的醋酸铵溶液为中性,故D错误;
故选C.
点评:本题考查了离子浓度大小比较、难溶物溶度积判断、盐的水解原理、酸碱混合的定性判断等知识,题目难度中等,试题涉及知识点较多,充分考查了学生的分析、理解能力及灵活应用所学知识解决实际问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
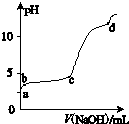 室温下,在一定体积的0.2mol?L-1 Al2(SO4)3溶液中,逐滴加入1.0mol?L-1 NaOH溶液,实验测得溶液pH随NaOH溶液体积的变化曲线如图所示,下列有关说法正确的是( )
室温下,在一定体积的0.2mol?L-1 Al2(SO4)3溶液中,逐滴加入1.0mol?L-1 NaOH溶液,实验测得溶液pH随NaOH溶液体积的变化曲线如图所示,下列有关说法正确的是( )| A、d点时,c(Na+):c (SO42-)=8:3 |
| B、b~c段,加入的OH-主要用于生成Al(OH)3沉淀 |
| C、a~b段,溶液无沉淀生成,Al3+浓度不变 |
| D、a点时,溶液呈酸性的原因是Al3+水解,离子方程式为:Al3++3 H2O?Al(OH)3+3 OH- |
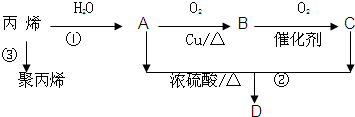
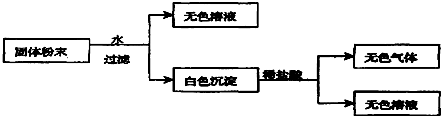

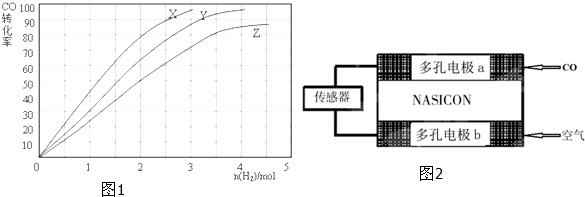
 用试纸检验气体性质是一种重要的实验方法.如图所示的实验中(可加热),下列试纸的选用、现象、对应结论都正确的一项是( )
用试纸检验气体性质是一种重要的实验方法.如图所示的实验中(可加热),下列试纸的选用、现象、对应结论都正确的一项是( )