题目内容
14.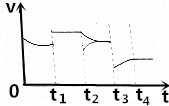 如图是反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)的正反应速率随时间的变化图象,在t1时反应达到平衡状态,然后改变一个条件,v正的变化如图所示,则下列说法正确的是( )
如图是反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)的正反应速率随时间的变化图象,在t1时反应达到平衡状态,然后改变一个条件,v正的变化如图所示,则下列说法正确的是( )| A. | t1时改变的条件是增大压强,且平衡没有移动 | |
| B. | t2时改变的条件时减小甲醇的浓度,且平衡正向移动 | |
| C. | t2时改变的条件是增大了氢气的浓度,且平衡正向移动 | |
| D. | t3是改变的条件是升高温度,且平衡正向移动 |
分析 根据外界条件的改变对化学反应速率及平衡移动的影响,结合图象分析,由图可知t1时正反应速率变大,但平衡未移动,因反应前后是气体体积减小的反应,故增大压强平衡会正向移动,t2改变条件时正反应速率不变,逆反应速率瞬间减小,应是减小生成物浓度,平衡正向移动.t3是改变的条件不可能是升高温度,因升高温度,正逆反应速率均会增大,由此分析解答.
解答 解:A.由图可知t1时正反应速率变大,但平衡未移动,因反应前后是气体体积减小的反应,则增大压强平衡会正向移动,故t1时改变的条件是加催化剂,故A错误;
B.t2改变条件时正反应速率不变,逆反应速率瞬间减小,应是减小生成物浓度,平衡正向移动,故B正确;
C.t2时改变的条件若是增大了氢气的浓度,则反应速率会瞬间增大,而图象中t2时改变的条件正反应速率不变,故C错误;
D.t3是改变的条件若是升高温度,正逆反应速率均会增大,而图象中速率减小,故D错误.
故选B.
点评 本题考查化学反应速率和化学平衡的图象问题,难度不大,注意条件变化对正反应速率随时间变化趋势及平衡移动的影响.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案
相关题目
5.下列各项正确的是( )
| A. | 酸性:H2SO4>H3PO4>H2SiO3 | B. | 还原性:Cl->Br->I- | ||
| C. | 氧化性:Na+<Mg2+<Al3+ | D. | 沸点:H2O<H2S<H2Se |
2.有关原电池的下列说法中正确的是( )
| A. | 在外电路中电子由正极流向负极 | |
| B. | 在原电池中负极发生还原反应 | |
| C. | 原电池中正极一定是不活泼金属 | |
| D. | 原电池工作时,阳离子向正极方向移动 |
1.已知液氨的性质与水相似,25℃时,NH3+NH3?NH${\;}_{4}^{+}$+NH${\;}_{2}^{-}$,NH${\;}_{4}^{+}$的平衡浓度为1×10-15mol•L-1,则下列说法中正确的是( )
| A. | 在液氨中加入NaNH2可使液氨的离子积变大 | |
| B. | 在液氨中加入NH4Cl可使液氨的离子积减小 | |
| C. | 在此温度下液氨的离子积为1×10-17 | |
| D. | 在液氨中放入金属钠,可生成NaNH2 |
19.在1.01×105Pa、150℃时,将3LC2H4、1LC2H2、1LC2H6与20LO2混合并点燃,完全反应后,恢复至原来状态,气体的体积是( )
| A. | 10L | B. | 15L | C. | 25L | D. | 30L |
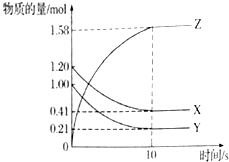 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,试回答下列问题:
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,试回答下列问题: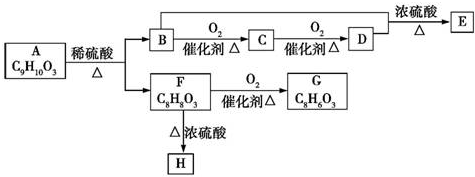
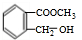 、
、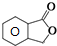 .
.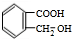 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2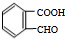 +2H2O.
+2H2O.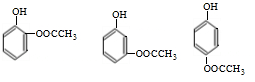 .
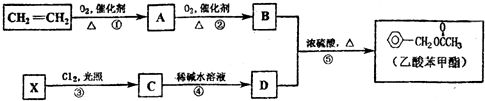
.
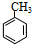 ,④的反应类型是取代反应.
,④的反应类型是取代反应.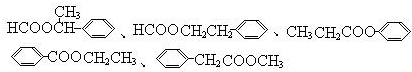 任意一种.
任意一种. .
.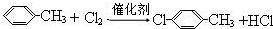 .
.