题目内容
5.用化学方法不能实现的是( )| A. | 生成一种新分子 | B. | 生成一种新离子 | ||
| C. | 生成一种新同位素 | D. | 生成一种新单质 |
分析 化学变化的实质是相互接触的分子间发生原子或电子的转换或转移,生成新的分子并伴有能量的变化的过程.
解答 解:根据化学变化的实质是相互接触的分子间发生原子或电子的转换或转移,生成新的分子并伴有能量的变化的过程,原子并没有发生变化,可知通过化学方法可以生产一种新分子,也可以生成一种新离子,还可生成一种新单质,具有一定数目的质子和一定数目的中字的原子称为核素,即核素的种类决定于原子核.而化学反应只是核外电子数目的变化,所以生成一种新同位素通过化学反应是不能实现的.
故选C.
点评 本题考查化学变化的实质,题目难度不大,要对化学变化的实质熟记并理解才能熟练运用.

练习册系列答案
相关题目
16.下列关于有机物的说法中正确的是( )
①棉花、蚕丝和人造丝的主要成分都是纤维素
②淀粉、油脂、蛋白质在一定条件下都能发生水解
③易溶于汽油、酒精、苯等有机溶剂的物质都是有机化合物
④除去乙酸乙酯中残留的乙酸,加过量饱和Na2CO3溶液振荡后,静置分液
⑤石油的分馏、裂化和煤的干馏都是化学变化
⑥聚碳酸酯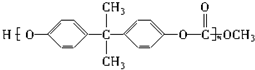 中含有
中含有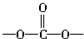 结构.
结构.
①棉花、蚕丝和人造丝的主要成分都是纤维素
②淀粉、油脂、蛋白质在一定条件下都能发生水解
③易溶于汽油、酒精、苯等有机溶剂的物质都是有机化合物
④除去乙酸乙酯中残留的乙酸,加过量饱和Na2CO3溶液振荡后,静置分液
⑤石油的分馏、裂化和煤的干馏都是化学变化
⑥聚碳酸酯
 中含有
中含有 结构.
结构.| A. | ②⑤ | B. | ②④⑥ | C. | ①②③⑥ | D. | ②④⑤ |
20.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | O2和O3的混合物共16g,其中所含氧原子数为NA | |
| B. | 1.0L 0.1mol/L的AlCl3溶液中含有的铝离子数为0.1NA | |
| C. | 28g乙烯中所含有共用电子对数目为4NA | |
| D. | 1mol金属钠完全转化为Na2O2所转移的电子数目为2NA |
10.室温下,下列溶液的离子浓度关系正确的是( )
| A. | pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合c(Na+)+c(H+)=c(OH-)+c( HC2O4-) | |
| B. | Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S) | |
| C. | NaHSO4溶液:c(H+)=c(SO42-)十c(OH-) | |
| D. | pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
17.如图是部分短周期元素最外层电子数与原子序数的关系图,下列说法正确的是( )


| A. | 原子半径:A<B<C<D | |
| B. | E、F和H三种元素相应的最高价氧化物对应水化物之间两两会发生反应 | |
| C. | 气态氢化物稳定性:D>I>G>H | |
| D. | E和C元素形成的化合物中只存在离子键 |
14.以下是一些物质的熔沸点数据(常压):
中国科学家用金属钠和CO2在一定条件下制得了金刚石:4Na+3CO2?2Na2CO3+C(s,金刚石)
完成下列填空:
(1)若反应在常压、890℃下进行,写出该反应的平衡常数表达式$\frac{1}{{c}^{4}(Na)×{c}^{3}(C{O}_{2})}$.
(2)请写出一条既能提高反应速率又能提高转化率的方法:增大压强
(3)890℃,下列关于该反应的说法正确的是b(选填序号).
a.容器内气体的平均式量不再变化,则反应一定达到平衡
b.容器内固体质量不再变化,则反应一定达到平衡
c.反应起始至平衡,气体的密度不断增大
d.反应起始至平衡,容器内的压强不断增大
(4)890℃,若该反应在10L密闭容器、常压下进行,反应4h,固体质量增加56克,则二氧化碳的反应速率为0.35mol/(L•h)
(5)若温度由890℃升高到1860℃,则容器内气体的平均相对分子质量将增大(选填“增大”“减小”“不变”),
(6)若反应后要得到纯净的金刚石,请写出必要的实验操作步骤.冷却后,将反应后容器中的固体取出,加水溶解、过滤、洗涤固体并烘干,可得纯净的金刚石
(7)在此反应中,同时还会有石墨生成,已知:C(s,石墨)?C(s,金刚石)-1.9KJ,若升高温度,生成的碳单质中,金刚石的含量将增大(选填“增大”“减小”“不变”).等物质的量的石墨和金刚石中,化学键的数目较多的是金刚石.
| 钠 | Na2CO3 | 金刚石 | 石墨 | |
| 熔点(℃) | 97.8 | 851 | 3550 | 3850 |
| 沸点(℃) | 882.9 | 1850(分解产生CO2) | ---- | 4250 |
完成下列填空:
(1)若反应在常压、890℃下进行,写出该反应的平衡常数表达式$\frac{1}{{c}^{4}(Na)×{c}^{3}(C{O}_{2})}$.
(2)请写出一条既能提高反应速率又能提高转化率的方法:增大压强
(3)890℃,下列关于该反应的说法正确的是b(选填序号).
a.容器内气体的平均式量不再变化,则反应一定达到平衡
b.容器内固体质量不再变化,则反应一定达到平衡
c.反应起始至平衡,气体的密度不断增大
d.反应起始至平衡,容器内的压强不断增大
(4)890℃,若该反应在10L密闭容器、常压下进行,反应4h,固体质量增加56克,则二氧化碳的反应速率为0.35mol/(L•h)
(5)若温度由890℃升高到1860℃,则容器内气体的平均相对分子质量将增大(选填“增大”“减小”“不变”),
(6)若反应后要得到纯净的金刚石,请写出必要的实验操作步骤.冷却后,将反应后容器中的固体取出,加水溶解、过滤、洗涤固体并烘干,可得纯净的金刚石
(7)在此反应中,同时还会有石墨生成,已知:C(s,石墨)?C(s,金刚石)-1.9KJ,若升高温度,生成的碳单质中,金刚石的含量将增大(选填“增大”“减小”“不变”).等物质的量的石墨和金刚石中,化学键的数目较多的是金刚石.
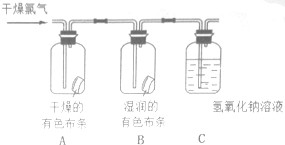 为了验证氯气的有关行政,某同学设计了如下的实验.
为了验证氯气的有关行政,某同学设计了如下的实验.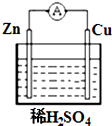 如图所示,在铜锌原电池中,以稀硫酸为电解质溶液:
如图所示,在铜锌原电池中,以稀硫酸为电解质溶液: