题目内容
16.在如图所示的原电池中,下列说法正确的是( )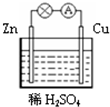
| A. | 负极反应为Cu-2e-═Cu2+ | B. | 正极反应为 Zn-2e-═Zn2+ | ||
| C. | Zn为负极,Cu为正极 | D. | 该装置能将电能转化为化学能 |
分析 该装置中,锌易失电子作负极,铜作正极,负极上失电子发生氧化反应,正极上得电子发生还原反应,电子从负极沿导线流向正极,以此解答该题.
解答 解:锌比铜活泼,则形成原电池反应时,锌为负极,电极反应式为:Zn-2e-═Zn2+,铜为正极,则A、B错误,C正确;
原电池工作时,负极发生氧化反应,正极发生还原反应,是将化学能转化为电能、故D错误,
故选C.
点评 本题考查了原电池原理,根据电极上得失电子判断正负极,再结合电极反应类型、电子流向来分析解答,熟记原电池原理,难点是电极反应式的书写.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
6.下列基团:-CH3、-OH、-COOH、-C6H5,相互两两组成的有机物有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
7.下列有关化学科学的说法中正确的是( )
| A. | 化学研究会造成严重的环境污染,最终人类会毁灭在化学物质中 | |
| B. | 化学研究的主要目的是认识分子 | |
| C. | 化学家可以制造出自然界中不存在的物质 | |
| D. | 俄国化学家门捷列夫提出了原子学说,为近代化学的发展奠定了基础 |
11.下列离子方程式改写成化学方程式正确的是( )
| A. | Cu2++2OH-=Cu(OH)2↓CuCO3+2NaOH═Cu(OH)2↓+Na2CO3 | |
| B. | CO32-+2H+=CO2↑+H2OBaCO3+2HCl═BaCl2+CO2↑+H2O | |
| C. | Ca2++CO32-=CaCO3↓Ca(NO3)2+Na2CO3═CaCO3↓+NaNO3 | |
| D. | H++OH-=H2OBa(OH)2+H2SO4═BaSO4↓+2H2O |
1.目前常用的垃圾处理方法主要有综合利用、卫生填埋、焚烧和堆肥.对这些处理方法的相关叙述中不正确的是( )
| A. | 可回收垃圾如纸类、金属、塑料、玻璃等,通过综合处理、回收利用,不仅可以减少污染,而且还可以节省资源 | |
| B. | 有害垃圾如废电池、废日光灯管、废水银温度计、过期药品等,这些垃圾需要进行特殊安全处理 | |
| C. | 厨余垃圾如剩菜剩饭、骨头、菜根菜叶等食品类废物,经生物技术就地处理堆肥,可以作为有机肥料,直接被农作物吸收和利用 | |
| D. | “白色污染”主要指的是我们日常用的塑料袋,它污染土壤的主要原因是不易被分解,影响正常的物质循环 |
8.已知aAn+bB(n+1)+ cCn-dD(n+1)-是具有相同电子层结构得短周期元素形成的简单离子.下列说法正确的是( )
| A. | 离子半径:C>D>A>B | B. | 核电核数:b>a>d>c | ||
| C. | 原子半径:A>B>D>C | D. | 元素的电负性:A>B>C>D |
 根据要求回答下列有关问题:
根据要求回答下列有关问题: .
. .
.