题目内容
1.实验室需要配制230mL 1mol•L-1的NaOH溶液,其实验步骤为:①计算所需氢氧化钠固体的质量为10.0g;
②称量氢氧化钠固体;
③将烧杯中的溶液注入容量瓶,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也注入容量瓶中,轻轻振荡;
④用适量的蒸馏水溶解称量好的氢氧化钠固体,冷却至室温;
⑤盖好瓶盖,摇匀;
⑥继续向容量瓶中加蒸馏水至刻度线下1-2cm时,改用胶头滴管滴加蒸馏水至凹液面最低点与刻度线相切.
根据上述信息回答问题:
(1)本实验操作步骤的正确顺序为①②④③⑥⑤.
(2)实验中需要用到容量瓶的规格为C.
A.300mL B.200mL C.250mL D.230mL
(3)如果实验遇到下列情况,对该氢氧化钠溶液的物质的量浓度有何影响(填“偏高”、“偏低”或“不变”).
①溶解氢氧化钠固体的烧杯没有洗涤偏低;
②搅拌以加速溶解时不小心洒出一小滴溶液偏低;
③定容时俯视观察液面偏高
(4)实验过程中如果出现如下情况该如何处理?
①定容后摇匀发现凹液面最低点低于刻度线无需处理;
②向容量瓶中转移溶液时不慎将少量溶液洒在容量瓶外重新配制.
分析 ①配制230mL 1mol•L-1的NaOH溶液,应选择250mL容量瓶,依据m=CVM计算需要溶质的质量;
⑥依据定容的正确操作解答;
(1)据配制溶液的实验操作过程进行实验步骤排序;
(2)依据配制溶液体积结合容量瓶规格选择合适容量瓶;
(3)根据c=$\frac{n}{V}$可得,一定物质的量浓度溶液配制的误差都是由溶质的物质的量n和溶液的体积V引起的,误差分析时,关键要看配制过程中引起n和V怎样的变化:若n比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;若n比理论值大,或V比理论值小时,都会使所配溶液浓度偏大.
(4)根据实验过程中出现任何误差引起浓度变化都要重新配制.
解答 解:①配制230mL 1mol•L-1的NaOH溶液,应选择250mL容量瓶,实际配制250mL溶液,需要溶质的质量m=CVM=1mol/L×40g/mol×0.25L=10.0g;
故答案为:10.0;
⑥定容时,向容量瓶中加入蒸馏水到刻度线下1-2cm时,改用胶头滴管滴加蒸馏水至凹液面最低点与刻度线相切;
故答案为:1-2;胶头滴管;
(1)配制1mol•L-1的NaOH溶液250mL,配制步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,用天平称量NaOH(用到药匙),在烧杯中稀释,并用玻璃棒搅拌,加速溶解,冷却后转移到250mL容量瓶中,并用玻璃棒引流,洗涤2-3次,并将洗涤液移入容量瓶,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀,所以操作顺序为:①②④③⑥⑤;
故答案为:①②④③⑥⑤;
(2)没有230mL容量瓶,需要选择250mL容量瓶,实际配制1mol•L-1的NaOH溶液250mL;
故答案为:C;
(3)①溶解氢氧化钠固体的烧杯没有洗涤,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低;
②搅拌以加速溶解时不小心洒出一小滴溶液,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低;
③定容时俯视观察液面,导致溶液体积偏小,溶液浓度偏高;
故选:偏低;偏低;偏高;
(4))①定容后摇匀发现凹液面最低点低于刻度线,是由于溶液粘在刻度线以上,属于正常现象,对溶液的物质的量浓度无影响,所以无需处理,
故答案为:无需处理;
②向容量瓶中转移溶液时不慎将少量溶液洒在容量瓶外不做处理,溶质的物质的量偏小,根据c=$\frac{n}{V}$可知该氢氧化钠的物质的量浓度偏低,
故答案为:重新配制.
点评 本题考查了配制一定物质的量浓度的溶液方法,题目难度不大,注意掌握配制一定浓度的溶液方法,能够根据配制步骤选用仪器,注意依据C=$\frac{n}{V}$进行误差分析的判断.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | CO2的电子式: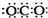 | B. | 核内有8个中子的碳原子:${\;}_{6}^{8}$C | ||
| C. | 甲烷的结构简式:CH4 | D. | 乙烯分子的球棍模型: |
| A. | σ键是轴对称的,π键是镜像对称的 | |
| B. | σ键是“头碰头”式重叠,π键是“肩并肩”式重叠 | |
| C. | σ键不能断裂,π键容易断裂 | |
| D. | H原子只能形成σ键,O原子可以形成σ键和π键 |
| A. | ③④⑤⑥⑦ | B. | ③④⑥ | C. | ④⑥⑦ | D. | ①③④⑤ |
①苯
②硝基苯③溴苯
④四氯化碳⑤溴乙烷
⑥乙酸乙酯.
| A. | ①⑥ | B. | ②③④ | C. | ②③④⑤ | D. | ③④⑤⑥ |
| A. | 乙酸和甲酸甲酯 | B. | 乙烷和乙醛 | ||
| C. | 甲醛和麦芽糖(C12H22O11) | D. | 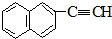 和 和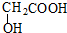 |
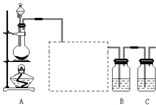 已知非金属单质硫(S)是淡黄色固体粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
已知非金属单质硫(S)是淡黄色固体粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题: