题目内容
设NA是阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下,22.4L乙醇中含有的氧原子数为NA |
| B、标准状况下,1.12L16O2和1.12L18O2均含有0.1NA个氧原子 |
| C、在Na2O2与水的反应中,生成lmolO2转移的电子数为 4×6.02×1023 |
| D、25℃时,pH=13的Ba(OH)2溶液中含有OH-数目为0.2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.标准状况下,乙醇的状态不是气体,不能使用标况下的气体摩尔体积计算乙醇的物质的量;
B.标准状况下1.12L气体的物质的量为0.05mol,0.05mol氧气中含有0.1mol氧原子;
C.过氧化钠中氧元素的化合价为-1价,生成1mol氧气转移了2mol电子;
D.没有告诉氢氧化钡溶液的体积,无法计算溶液中氢氧根离子的数目.
B.标准状况下1.12L气体的物质的量为0.05mol,0.05mol氧气中含有0.1mol氧原子;
C.过氧化钠中氧元素的化合价为-1价,生成1mol氧气转移了2mol电子;
D.没有告诉氢氧化钡溶液的体积,无法计算溶液中氢氧根离子的数目.
解答:
解:A.标况下乙醇不是气体,不能使用标况下的气体摩尔体积计算22.4L乙醇的物质的量,故A错误;
B.标况下1.12L氧气的物质的量为0.05mol,0.05mol两种氧气中都含有0.1mol氧原子,含有0.1NA个氧原子,故B正确;
C.过氧化钠与水反应生成1mol氧气转移了2mol电子,转移的电子数为2×6.02×1023,故C错误;
D.缺少氢氧化钡溶液的体积,无法计算溶液中氢氧根离子的物质的量及数目,故D错误;
故选B.
B.标况下1.12L氧气的物质的量为0.05mol,0.05mol两种氧气中都含有0.1mol氧原子,含有0.1NA个氧原子,故B正确;
C.过氧化钠与水反应生成1mol氧气转移了2mol电子,转移的电子数为2×6.02×1023,故C错误;
D.缺少氢氧化钡溶液的体积,无法计算溶液中氢氧根离子的物质的量及数目,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的综合应用,题目难度不大,注意掌握物质的量与阿伏伽德罗常数、摩尔质量、气体摩尔体积等物理量之间关系,明确标况下气体摩尔体积的使用条件,选项D为易错点,注意题中缺少溶液的体积.

练习册系列答案
相关题目
同温同压下,下列气体的密度最大的是( )
| A、F2 |
| B、Cl2 |
| C、HCl |
| D、CO2 |
用惰性电极电解下列溶液,一段时间后,阴极质量增加,电解液的pH下降的是( )
①CuSO4 ②BaCl2 ③AgNO3 ④H2SO4.
①CuSO4 ②BaCl2 ③AgNO3 ④H2SO4.
| A、①② | B、②④ | C、①④ | D、①③ |
下列各组有机物只用一种试剂无法鉴别的是( )
| A、乙醇、乙酸、乙酸乙酯 |
| B、苯酚、己烯、四氯化碳 |
| C、对二甲苯、苯、环己烷 |
| D、乙醛、乙酸、葡萄糖 |
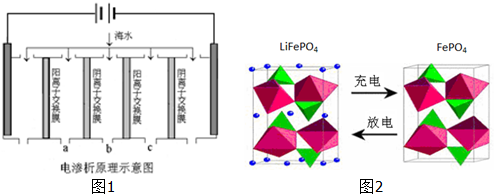
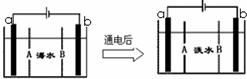 电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示.已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极.下列叙述中正确的是
电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示.已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极.下列叙述中正确的是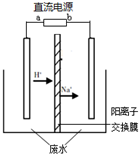 电解CH3CHO是有毒物质,易溶于水,含高浓度CH3CHO的废水可以用隔膜电解法处理,总反应为:
电解CH3CHO是有毒物质,易溶于水,含高浓度CH3CHO的废水可以用隔膜电解法处理,总反应为: