题目内容
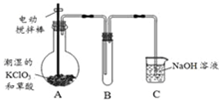 二氧化氯(ClO2)在常温下是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用如图所示装置模拟工业制取并收集ClO2.
二氧化氯(ClO2)在常温下是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用如图所示装置模拟工业制取并收集ClO2.(1)A中反应产物有K2CO3、ClO2和CO2等,请写出该反应的化学方程式:
(2)A必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯、
(3)反应后在装置C中可得NaClO2溶液.已知NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2?3H2O,在温度高于38℃时析出晶体是NaClO2.请补充从NaClO2溶液中制得NaClO2晶体的操作步骤:
①
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液.为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10.00mL,稀释成100.00mL试样;量取V1 mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入淀粉指示剂,用c mol/L Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL.(已知2Na2S2O3+I2═Na2S4O6+2NaI)
①配制100mL c mol/L Na2S2O3标准溶液时,用到的玻璃仪器除烧杯、量筒、玻璃棒外还有:
②滴定过程中至少需进行两次平行测定的原因是
③写出步骤2中发生反应的离子方程式
④原ClO2溶液的浓度为
⑤若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果
考点:制备实验方案的设计,探究物质的组成或测量物质的含量
专题:实验探究和数据处理题,实验设计题
分析:(1)根据反应物、产物和反应条件写出反应方程式;
(2)测量温度的仪器是温度计,二氧化氯的熔点较低,为收集二氧化氯,应在较低温度下进行;
(3)从溶液中制取溶质,一般采用蒸发结晶、过滤、洗涤、干燥的方法;
(4)①根据配制一定物质的量浓度的溶液使用的仪器解答;
②多次实验可以减少误差;
③二氧化氯具有氧化性,在酸性环境下,能将碘离子氧化;
④根据关系式2ClO2~5I2~10Na2S2O3计算c(ClO2);
⑤根据实验操作中滴定液体积大小的影响来回答判断.
(2)测量温度的仪器是温度计,二氧化氯的熔点较低,为收集二氧化氯,应在较低温度下进行;
(3)从溶液中制取溶质,一般采用蒸发结晶、过滤、洗涤、干燥的方法;
(4)①根据配制一定物质的量浓度的溶液使用的仪器解答;
②多次实验可以减少误差;
③二氧化氯具有氧化性,在酸性环境下,能将碘离子氧化;
④根据关系式2ClO2~5I2~10Na2S2O3计算c(ClO2);
⑤根据实验操作中滴定液体积大小的影响来回答判断.
解答:
解:(1)加热60℃,氯酸钾和草酸反应生成碳酸钾、二氧化碳、二氧化氯和水,反应方程式为:2KClO3+H2C2O4
K2CO3+CO2↑+2ClO2↑+H2O,
故答案为:2KClO3+H2C2O4
K2CO3+CO2↑+2ClO2↑+H2O;
(2)要控制温度必须使用温度计测量温度,二氧化氯的熔点较低,为收集二氧化氯,应在较低温度下进行,所以应该采用冰水浴,故答案为:温度计;使ClO2充分冷凝,减少挥发;
(3)从溶液中制取溶质,一般采用蒸发结晶、过滤、洗涤、干燥的方法,为防止析出晶体NaClO2?3H2O,应趁热过滤,
故答案为:蒸发浓缩结晶;趁热过滤;
(4)①配制100mL溶液用到的仪器有托盘天平、药匙、玻璃棒、胶头滴管、烧杯、100mL容量瓶、量筒(可用可不用),故还需要的玻璃仪器有:100mL容量瓶、胶头滴管,
故答案为:100ml容量瓶、胶头滴管;
②为减少实验误差,应采用多次实验的方法,故答案为:减少误差;
③二氧化氯具有氧化性,在酸性环境下,能将碘离子氧化,反应的原理方程式为:2ClO2+10I-+8H+=2Cl-+5I2+4H2O,故答案为:2ClO2+10I-+8H+=2Cl-+5I2+4H2O;
④设原ClO2溶液的浓度为x,
2ClO2~5I2~10Na2S2O3
2mol 10mol
1×10-3cV2mol
x=
g/L=
g/L,
故答案为:
g/L;
⑤若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则相当于消耗的滴定液的体积偏大,所以测定结果偏大,若滴定开始仰视读数,滴定终点时正确读数,相当于消耗的滴定液体积偏小,所以结果偏小,故答案为:偏高;偏小.
| ||
故答案为:2KClO3+H2C2O4
| ||
(2)要控制温度必须使用温度计测量温度,二氧化氯的熔点较低,为收集二氧化氯,应在较低温度下进行,所以应该采用冰水浴,故答案为:温度计;使ClO2充分冷凝,减少挥发;
(3)从溶液中制取溶质,一般采用蒸发结晶、过滤、洗涤、干燥的方法,为防止析出晶体NaClO2?3H2O,应趁热过滤,
故答案为:蒸发浓缩结晶;趁热过滤;
(4)①配制100mL溶液用到的仪器有托盘天平、药匙、玻璃棒、胶头滴管、烧杯、100mL容量瓶、量筒(可用可不用),故还需要的玻璃仪器有:100mL容量瓶、胶头滴管,
故答案为:100ml容量瓶、胶头滴管;
②为减少实验误差,应采用多次实验的方法,故答案为:减少误差;
③二氧化氯具有氧化性,在酸性环境下,能将碘离子氧化,反应的原理方程式为:2ClO2+10I-+8H+=2Cl-+5I2+4H2O,故答案为:2ClO2+10I-+8H+=2Cl-+5I2+4H2O;
④设原ClO2溶液的浓度为x,
2ClO2~5I2~10Na2S2O3
2mol 10mol
| 10-2x×V1×10-3 |
| 10-1 |
x=
| 2cV2 |
| V1 |
| 135cV2 |
| V1 |
故答案为:
| 135cV2 |
| V1 |
⑤若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则相当于消耗的滴定液的体积偏大,所以测定结果偏大,若滴定开始仰视读数,滴定终点时正确读数,相当于消耗的滴定液体积偏小,所以结果偏小,故答案为:偏高;偏小.
点评:本题考查实验方案的设计,同时考查学生分析问题、解决问题的能力,明确物质的性质是解本题关键,难度较大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某有机物的结构简式为,它在一定条件下可能发生的反应有①加成 ②水解 ③酯化 ④氧化 ⑤中和 ⑥消去( )
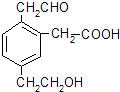

| A、②③④ | B、①③④⑤ |
| C、①③④⑤⑥ | D、①②③④⑤⑥ |