题目内容
向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L.向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g.再将得到的沉淀灼烧至质量不再改变为止,得到固体p g.则下列关系不正确的是( )
| A、n=m+17Vc | ||||
B、c=
| ||||
C、p=m+
| ||||
D、
|
考点:有关混合物反应的计算
专题:
分析:A.沉淀为氢氧化镁、氢氧化铝,其质量等于金属的质量与含有的氢氧根离子的质量之和,根据n=cVM计算氢氧根离子的质量;
B.根据n=
计算氢气的物质的量,根据电荷守恒可知,氢氧化镁、氢氧化铝沉淀中含有n(OH-),等于金属提供的电子的物质的量,等于生成氢气的获得的电子的物质的量,据此计算氢氧根离子的物质的量,再根据c=
计算氢氧化钾的物质的量浓度;
C.由Mg(OH)2
MgO+H2O,2Al(OH)3
Al2O3+3H2O可知,沉淀灼烧生成氧化镁与氧化铝,二者质量等于金属质量与氧原子的质量之和,由方程式可知氧原子的物质的量等于氢氧根离子物质的量的一半,据此计算;
D.按照极值方法计算,若m g全是镁,计算生成得到的氧化镁质量,若m g全是铝,计算得到的氧化铝的质量,实际固体的质量介于二者之间.
B.根据n=
| V |
| Vm |
| n |
| V |
C.由Mg(OH)2
| ||
| ||
D.按照极值方法计算,若m g全是镁,计算生成得到的氧化镁质量,若m g全是铝,计算得到的氧化铝的质量,实际固体的质量介于二者之间.
解答:
解:A.沉淀为氢氧化镁、氢氧化铝,其质量等于金属的质量与含有的氢氧根离子的质量之和,故n=m+c×V×10-3×17=m+
,故A错误;
B.根据电荷守恒可知,氢氧化镁、氢氧化铝沉淀中含有n(OH-),等于金属提供的电子的物质的量,等于生成氢气的获得的电子的物质的量,故生成的氢气的物质的量等于参加反应的碱的物质的量的一半,故
×2=cmol/L×V×10-3L,整理得c=
,故B正确;
C.选项中p为生成的氧化物的质量,由Mg(OH)2
MgO+H2O,2Al(OH)3
Al2O3+3H2O可知,氧化物的质量等于金属质量与氧原子的质量之和,由方程式可知氧原子的物质的量等于氢氧根离子物质的量的一半,故p=m+c×V×10-3×
×16=m+
,故C正确;
D.得到的氧化物为氧化镁,根据元素守恒,则质量为P=
×40=
,若mg全是铝,得到的氧化物为氧化铝,根据元素守恒,则质量为p=
×
×102=
,氧化物质量介于二者之间,即
<p<
,故D正确;
故选A.
| 17Vc |
| 1000 |
B.根据电荷守恒可知,氢氧化镁、氢氧化铝沉淀中含有n(OH-),等于金属提供的电子的物质的量,等于生成氢气的获得的电子的物质的量,故生成的氢气的物质的量等于参加反应的碱的物质的量的一半,故
| bL |
| 22.4L/mol |
| 1000b |
| 11.2V |
C.选项中p为生成的氧化物的质量,由Mg(OH)2
| ||
| ||
| 1 |
| 2 |
| cV |
| 125 |
D.得到的氧化物为氧化镁,根据元素守恒,则质量为P=
| m |
| 24 |
| 5m |
| 3 |
| m |
| 27 |
| 1 |
| 2 |
| 17m |
| 9 |
| 5m |
| 3 |
| 17m |
| 9 |
故选A.
点评:本题综合考查镁铝元素单质及化合物的性质、混合物的有关计算,注意利用方程式与电子转移守恒寻找关系解答,题目计算量较大,且为无数据计算,难度较大.

练习册系列答案
相关题目
实验室制乙酸乙酯1mL后,沿器壁加入紫色石蕊试液0.5mL,这时石蕊试液将存在于饱和碳酸钠溶液层与乙酸乙酯层之间(整个过程不振荡).对可能出现的现象,下列叙述中正确的是( )
| A、石蕊层仍为紫色,有机层无色 |
| B、石蕊层为三层环,由上而下是红、紫、红 |
| C、石蕊层有两层,上层为紫色,下层为蓝色 |
| D、石蕊层为三层环,由上而下是蓝、紫、红 |
下列有关NaCl在生物技术实践中的应用,正确的是( )
| A、在配制牛肉膏蛋白胨固体培养基时,需加入琼脂,不需要添加NaCl |
| B、利用DNA在不同浓度的NaCl溶液中的溶解度不同,粗提取DNA |
| C、在腐乳制作过程中,装瓶时需逐层等量加入NaCl,以防杂菌污染 |
| D、将哺乳动物的成熟红细胞浸泡于0.9%的NaCl溶液中,用以制备纯净的细胞膜 |
三氯生是一种抗菌剂,其结构如图所示,遇含氯自来水能生成有毒的三氯甲烷.下列说法不正确的是( ) 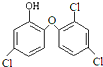

| A、三氯生的分子式是C12H7Cl3O2 |
| B、三氯甲烷与甲烷均无同分异构体 |
| C、1 mol三氯生最多能与6 mol H2反应 |
| D、1 mol三氯生最多能与4mol NaOH反应 |
下列关于煤的干馏的叙述中,正确的是( )
| A、煤加强热而分解的过程叫做煤的干馏 |
| B、煤干馏的目的是得到冶金用的优质焦炭 |
| C、煤的干馏和石油的分馏的本质差别是:干馏是物理变化,而分馏是化学变化 |
| D、工业上苯等芳香烃原料可由煤干馏得到,其存在于干馏所得的焦炉气中 |
有下列三个反应:下列说法正确的是( )
①Cl2+FeI2═FeCl2+I2
②2Fe2++Br2═2Fe3++2Br-
③Co2O3+6HCl═2CoCl2+Cl2↑+3H2O.
①Cl2+FeI2═FeCl2+I2
②2Fe2++Br2═2Fe3++2Br-
③Co2O3+6HCl═2CoCl2+Cl2↑+3H2O.
| A、反应①②③中的氧化产物分别是I2、Fe3+、CoCl2 |
| B、根据以上方程式可以得到氧化性:Cl2>Fe3+>Co2O3 |
| C、在反应③中当1 mol Co2O3参加反应时,2 mol HCl被氧化 |
| D、可以推理得到Cl2+FeBr2═FeCl2+Br2 |
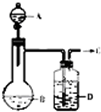 为了制取干燥纯净的气体C,可用如下图所示装置.生成C的速度可通过调节滴入液体A的速度的方法来控制,已知C是一种无色无味、不能使酸碱指示剂变色,也不会在空气中燃烧的气体.
为了制取干燥纯净的气体C,可用如下图所示装置.生成C的速度可通过调节滴入液体A的速度的方法来控制,已知C是一种无色无味、不能使酸碱指示剂变色,也不会在空气中燃烧的气体.