题目内容
为了探究钠与氧气的反应,某同学做了以下实验:
①用刀切开金属钠,观察切开的金属钠表面发生的变化.
②把一小块钠放在石棉网上加热,观察发生的现象.
请预测实验现象,并分析可能得到的结论.
①用刀切开金属钠,观察切开的金属钠表面发生的变化.
②把一小块钠放在石棉网上加热,观察发生的现象.
请预测实验现象,并分析可能得到的结论.
| 实验现象 | 结论 | |
| 实验① | ||
| 实验② |
考点:碱金属及其化合物的性质实验
专题:实验题
分析:①钠为银白色金属,性质活泼,易与空气中氧气反应生成Na2O;
②将金属钠放在氧气中燃烧,金属钠先熔化,然后燃烧,火焰呈黄色,生成物是淡黄色过氧化钠固体.
②将金属钠放在氧气中燃烧,金属钠先熔化,然后燃烧,火焰呈黄色,生成物是淡黄色过氧化钠固体.
解答:
解:解:①钠为银白色金属,性质活泼,易与空气中氧气反应生成白色的Na2O,所以表面变暗,
反应的方程式为4Na+O2═2Na2O,故答案为:钠为银白色金属,银白色迅速转变为灰色;金属钠很活泼,在常温下与氧气反应;
②将金属钠放在氧气中燃烧,金属钠的熔点较低,看到金属钠先熔化,然后燃烧,燃烧时火焰呈黄色,生成淡黄色固体,化学方程式为2Na+O2
Na2O2
故答案为:钠融化成小球,燃烧发出黄色火焰,生成淡黄色的固体,钠加热条件下与氧气反应生成过氧化钠.
反应的方程式为4Na+O2═2Na2O,故答案为:钠为银白色金属,银白色迅速转变为灰色;金属钠很活泼,在常温下与氧气反应;
②将金属钠放在氧气中燃烧,金属钠的熔点较低,看到金属钠先熔化,然后燃烧,燃烧时火焰呈黄色,生成淡黄色固体,化学方程式为2Na+O2
| ||
故答案为:钠融化成小球,燃烧发出黄色火焰,生成淡黄色的固体,钠加热条件下与氧气反应生成过氧化钠.
点评:本题考查学生金属钠的性质,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
下列操作不能达到实验目的或错误的是( )
A、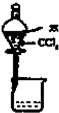 分离CCl4和水 |
B、 溶液的配制 |
C、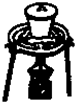 灼烧碳酸钙 |
D、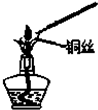 Na2CO3的焰色反应 |
 生理盐水,是指生理学实验或临床上常用的渗透压与动物或人体血浆的渗透压相等的氯化钠溶液.浓度:用于两栖类动物时是0.67~0.70%,用于哺乳类动物和人体时是0.85~0.9%人们平常点滴用的氯化钠注射液浓度是0.9%,可以当成生理盐水来使用.请回答下面有关点滴用的氯化钠注射液的问题.
生理盐水,是指生理学实验或临床上常用的渗透压与动物或人体血浆的渗透压相等的氯化钠溶液.浓度:用于两栖类动物时是0.67~0.70%,用于哺乳类动物和人体时是0.85~0.9%人们平常点滴用的氯化钠注射液浓度是0.9%,可以当成生理盐水来使用.请回答下面有关点滴用的氯化钠注射液的问题.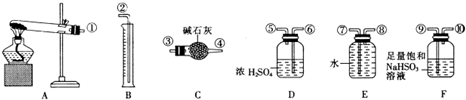
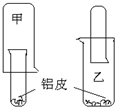 为了适应“低碳生活”,某化学兴趣小组用铝制废牙膏皮、一大一小两种试管和稀硫酸来制取并收集一试管氢气.据此完成下列要求.
为了适应“低碳生活”,某化学兴趣小组用铝制废牙膏皮、一大一小两种试管和稀硫酸来制取并收集一试管氢气.据此完成下列要求.