题目内容
17.常温下将稀KOH溶液和稀CH3COOH溶液混合,不可能出现的结果是( )| A. | pH>7,且c(OH?)>c(K+)>c(H+)>c(CH3COO?) | B. | pH>7,且c(K+)+c(H+)=c(CH3COO?)+c(OH?) | ||
| C. | pH<7,且c(CH3COO?)>c(H+)>c(K+)>c(OH?) | D. | pH=7,且c(CH3COO?)=c(K+)>c(H+)=c(OH?) |
分析 A、稀KOH溶液和稀CH3COOH溶液混合,pH>7,说明溶液可以是醋酸钾溶液,或者是氢氧化钾和醋酸钾的混合物,据此确定离子浓度的大小;
B、稀KOH溶液和稀CH3COOH溶液混合,不管溶液显示什么性,溶液中均存在电荷守恒;
C、稀KOH溶液和稀CH3COOH溶液混合,pH<7,说明醋酸剩余;
D、稀KOH溶液和稀CH3COOH溶液混合,pH=7,溶液显示中性,根据电荷守恒来回答.
解答 解:A、稀KOH溶液和稀CH3COOH溶液混合,pH>7,说明溶液可以是氢氧化钾和醋酸钾的混合物,则c(K+)>c(OH-)>c(CH3COO-)>c(H+),还可以是醋酸钾溶液,c(K+)>c(CH3COO-)>c(OH-)>c(H+),故A错误;
B、稀KOH溶液和稀CH3COOH溶液混合,溶液中存在电荷守恒:c(K+)+c(H+)=c(CH3COO-)+c(OH-),故B正确;
C、稀KOH溶液和稀CH3COOH溶液混合,pH<7,说明醋酸剩余,所得溶液是等浓度的醋酸和醋酸钾的混合物,醋酸的电离大于醋酸根离子水解,或是醋酸浓度大于醋酸钾浓度,即c(CH3COO-)>c(H+)>c(K+)>c(OH-)存在,故C正确;
D、稀KOH溶液和稀CH3COOH溶液混合,pH=7,溶液显示中性,c(H+)=c(OH-),根据电荷守恒c(CH3COO-)+c(OH-)=c(K+)+c(H+),所以c(CH3COO-)=c(K+),此时一定存在:c(CH3COO-)=c(K+)>c(H+)=c(OH-),故D正确.
故选A.
点评 本题是一道关于离子浓度大小比较以及离子浓度之间关系的综合知识题目,考查学生分析和解决问题的能力,注意三大守恒思想的灵活应用是关键,综合性较强,难度中等.

练习册系列答案
相关题目
5.合成氨反应N2(g)+3H2(g)?2NH3(g),已知H-H键能为436kJ/mol,N≡N键能为945kJ/mol,N-H键能为39IkJ/mol,则该反应的反应热△H为( )
| A. | 1471kJ/mol | B. | -1471kJ/mol | C. | 93kJ/mol | D. | -93kJ/mol |
12.工业上获得大量的乙烯、丙烯和甲烷,采用的方法是( )
| A. | 石油分馏 | B. | 石油裂化 | C. | 石油裂解 | D. | 通过沼气池制取 |
2.下列说法正确的是( )
①离子化合物含离子键,也可能含极性键或非极性键
②共价化合物含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
⑥离子化合物在熔融状态能导电.
①离子化合物含离子键,也可能含极性键或非极性键
②共价化合物含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
⑥离子化合物在熔融状态能导电.
| A. | ①③⑥ | B. | ②④⑥ | C. | ②③④ | D. | ①③⑤ |
9.关于如图所示的原电池,下列说法正确的是( )
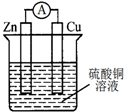

| A. | 电子从锌电极通过电流表流向铜电极 | |
| B. | 锌电极发生还原反应,铜电极发生氧化反应 | |
| C. | 反应后,锌电极的质量减小 | |
| D. | 铜电极作正极,发生的电极反应为2H++2e-═H2↑ |
6.下列有关三氧化硫的说法中,正确的是( )
| A. | 三氧化硫极易溶于水,且与水反应生成H2SO3 | |
| B. | SO3属于酸性氧化物 | |
| C. | 硫粉在过量的氧气中燃烧生成SO3 | |
| D. | SO2、SO3均具有漂白性,能使紫色石蕊溶液褪色 |
7.NH3和BF3可以通过配位键形成化合物NH3•BF3.下列说法正确的是( )
| A. | NH3、BF3两分子都是极性分子 | |
| B. | NH3、BF3两分子的中心原子采取的都是sp3杂化 | |
| C. | 形成配合物时NH3中N原子提供的是孤对电子,BF3中B原子提供空轨道 | |
| D. | 形成配合物时BF3中B原子提供的是孤对电子,NH3中N原子提供空轨道 |
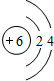 .
.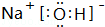 ,其中存在的化学键有离子键、共价键.
,其中存在的化学键有离子键、共价键.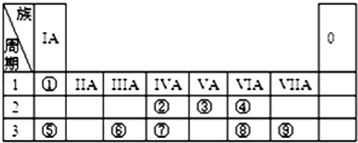
 ,Y中含有的化学键类型是共价键.
,Y中含有的化学键类型是共价键.