题目内容
用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.0.1molCl2常温下与过量NaOH溶液反应转移电子总数为 0.1NA
B.25℃时, pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA
C.0.25mol Na2O2中含有的阴离子数为0.5 NA
D.1L0.1mol·L-1的硫化钠溶液中硫离子数目为0.1NA
A
【解析】
试题分析:A、Cl2与NaOH反应生成NaCl、NaClO和H2O,Cl2与电子转移数目的对应关系为:Cl2 ~ e?,所以0.1molCl2常温下与过量NaOH溶液反应转移电子总数为 0.1NA,正确;B、没有指明溶液的体积,无法求算离子数目,错误;C、O22?为1个离子,所以0.25mol Na2O2中含有的阴离子数为0.25 NA,错误;D、S2?发生水解反应,所以1L0.1mol·L-1的硫化钠溶液中硫离子数目小于0.1NA,错误。
考点:本题考查 阿伏伽德罗常数的应用。

练习册系列答案
相关题目
下列实验“操作和现象”与“结论”对应关系正确的是
| 操作和现象 | 结论 |
A | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体 | HNO3分解生成了NO2 |
B | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热,没有红色沉淀生成 | 淀粉没有水解成葡萄糖 |
C | 向饱和Na2CO3溶液中通入足量CO2 ,溶液变浑浊 | 析出了NaHCO3 |
D | 向无水乙醇中加入浓H2SO4,加热至170℃产生的气体通入酸性KMnO4溶液,红色褪去 | 使溶液褪色的气体是乙烯 |

 2NH3
2NH3 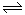 4NH3(g)+3O2(g) △H=Q ①
4NH3(g)+3O2(g) △H=Q ①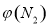 与反应温度T的关系曲线如下图所示,则上述反应的Q________0(填“>”、“<”或“=”)。
与反应温度T的关系曲线如下图所示,则上述反应的Q________0(填“>”、“<”或“=”)。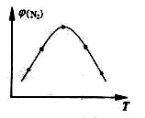
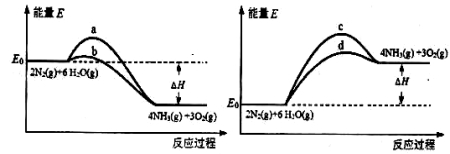
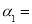 ______________。
______________。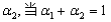 时,则起始时NH3的物质的量
时,则起始时NH3的物质的量 _________mol。
_________mol。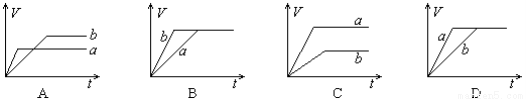 、
、