题目内容
将一充满NO2和NO的混合气体的试管倒立于水槽中,充分反应后,若水上升到
处,则原混合气体中NO2和NO的体积比是 .
| 1 |
| 4 |
考点:化学方程式的有关计算
专题:
分析:NO2和NO的混合气体通入倒立于水槽中盛满水的试管中,发生反应3NO2+H2O=2HNO3+NO,水上升到
处,则试管中
体积为NO,结合体积差计算.
| 1 |
| 4 |
| 3 |
| 4 |
解答:
解:发生反应3NO2+H2O=2HNO3+NO,水上升到
处,则试管中
体积为NO,
设NO2和NO混合气体体积为V,NO2为x,则
3NO2+H2O=2HNO3+NO△V
3 1 2
x
V
=
,解得x=
V,
则原混合气体中NO为V-
V=
V,
所以原混合气体中NO2和NO的体积比是3:5,
故答案为:3:5.
| 1 |
| 4 |
| 3 |
| 4 |
设NO2和NO混合气体体积为V,NO2为x,则
3NO2+H2O=2HNO3+NO△V
3 1 2
x
| 1 |
| 4 |
| 3 |
| x |
| 2 | ||
|
| 3 |
| 8 |
则原混合气体中NO为V-
| 3 |
| 8 |
| 5 |
| 8 |
所以原混合气体中NO2和NO的体积比是3:5,
故答案为:3:5.
点评:本题考查化学反应方程式的计算,为高频考点,把握发生的化学反应及差量法计算为解答的关键,注意氮的氧化性的性质,题目难度不大.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
在一定温度下,向某固定容积的密闭容器中加入1mol N2和3mol H2,发生如下反应:N2(g)+3H2(g)?2NH3(g).此反应达到平衡的标志是( )
| A、容器内气体密度不再发生变化 |
| B、容器内各物质的浓度不再发生变化 |
| C、正反应和逆反应都已停止 |
| D、单位时间消耗0.1mol N2的同时生成0.2mol NH3 |
下列说法正确的是( )
| A、油脂属于酯类,可分为油和脂肪 |
| B、油脂、蛋白质都是由C、H、O三种元素组成的 |
| C、糖类、油脂、蛋白质、塑料、橡胶、纤维都是高分子化合物 |
| D、糖类、油脂、蛋白质都能发生水解反应 |
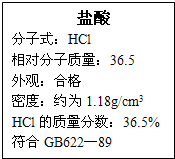 右图为某市售盐酸试剂瓶标签上的部分数据,通过计算回答:
右图为某市售盐酸试剂瓶标签上的部分数据,通过计算回答: