题目内容
15.下列反应属于离子反应的是( )| A. | H2和O2反应生成水 | B. | CuO投入稀硫酸中 | ||
| C. | 高温煅烧石灰石制CO2 | D. | NaOH溶液和K2SO4溶液混合 |
分析 有离子参加的反应属于离子反应,一般在溶液中进行,以此解答该题.
解答 解:H2和O2反应、高温煅烧石灰石制CO2不是溶液中的反应,不属于离子反应,CuO投入稀硫酸中,CuO与氢离子参加反应,为离子反应,NaOH溶液和K2SO4溶液混合不符合复分解反应的条件,不能进行.
故选B.
点评 本题考查离子反应,侧重于学生的分析能力的考查,为高考高频考点,注意把握反应的特点和离子反应的条件,难度不大.

练习册系列答案
相关题目
16.把0.05molNaOH固体分别加入到100ml下列液体中,溶液导电能力变化最小的是( )
| A. | 自来水 | B. | 0.5mol/L盐酸 | C. | 0.5mol/LHAc溶液 | D. | 0.5mol/LKCl溶液 |
20.碱性锌锰电池比酸性锌猛电池性能好,放电电流大,碱性锌锰电池的总反应式:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,下列有关碱性锌锰电池的说法正确的是( )
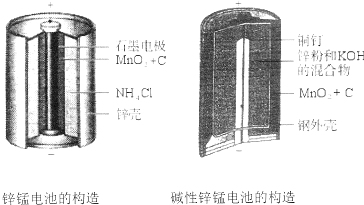

| A. | 该电池反应中二氧化锰起催化作用 | |
| B. | 电池负极反应式为:2MnO2+2e-+2H2O═2MnOOH+2OH- | |
| C. | 当0.1molZn完全反应时,流经电池内部的电子个数为1.204×1023 | |
| D. | 碱性锌锰电池用锌粉替代了原锌锰电池的锌壳,增大了反应物的接触面积,加快了反应速率,故放电电流大 |
7.下列说法正确的是( )
| A. | 检验NH4+时,往试样中加入NaOH溶液,微热,用湿润的蓝色石蕊试纸检验逸出的气体 | |
| B. | 碘易升华,可用加热升华法除去NH4Cl混有的I2 | |
| C. | 铁在硫蒸气中燃烧生成Fe2S3 | |
| D. | 在过氧化钠与水的反应,毎生成0.1mol氧气,转移电子的数目为0.2NA |
4.为了从海带浸取液中提取碘,某同学设计了如图实验方案:下列说法正确的是( )
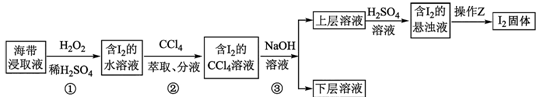

| A. | ①中反应的离子方程式:2I-+H2O2═I2+2OH- | |
| B. | ②中分液时含I2的CCl4溶液从分液漏斗上口倒出 | |
| C. | ③中得到的上层溶液中含有I- | |
| D. | 操作Z的名称是加热 |
5.下列各组物质中,所含分子数相同的是( )
| A. | 1 g H2和1 g O2 | |
| B. | 5.6 L N2(标准状况)和22 g CO2 | |
| C. | 9 g H2O(非标准状况)和11.2 L(标准状况)Cl2 | |
| D. | 22.4 L H2(标准状况)和0.1 mol N2 |
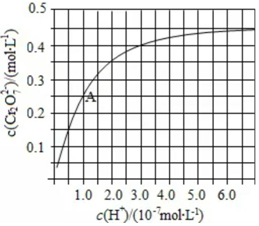 元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4-(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4-(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题: