题目内容
I.已知:C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别如下:
C(s)+O2(g)=CO2(g)△H=-394kJ/mol①
2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol②
2H2(g)+O2(g)=2H2O(g)△H=-484kl/mol③
(1)试写出由C(s)与水蒸气在高温条件下反应生成氢气和一氧化碳的热化学方程式:______________________。
(2)若利用上述反应②设计一个燃料电池,如用氢氧化钾溶液作电解质溶液,用多孔石墨作电极,写出负极的电极反应式:________________。
Ⅱ.如图所示,横坐标为溶液的pH,纵坐标为Al3+或[Al(OH)4]-的物质的量浓度的对数,回答下列问题。
C(s)+O2(g)=CO2(g)△H=-394kJ/mol①
2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol②
2H2(g)+O2(g)=2H2O(g)△H=-484kl/mol③
(1)试写出由C(s)与水蒸气在高温条件下反应生成氢气和一氧化碳的热化学方程式:______________________。
(2)若利用上述反应②设计一个燃料电池,如用氢氧化钾溶液作电解质溶液,用多孔石墨作电极,写出负极的电极反应式:________________。
Ⅱ.如图所示,横坐标为溶液的pH,纵坐标为Al3+或[Al(OH)4]-的物质的量浓度的对数,回答下列问题。

(3)往0.1mol/L的AlCl3溶液中加入氨水,调节溶液的pH 为6,反应的离子方程式为_____________________;此时改加NaOH溶液,至溶液的pH=10,反应的离子方程式可以表示为_________________。
(4)某溶液中含有Al3+,为提纯Al3+可以控制溶液的pH范围为______________。
(5)从图中选取适当的数据计算Al(OH)3的溶度积(Ksp)=________________
(6)用石墨电极电解AlCl3溶液,试写出电解初始阶段的化学方程式:______________。
(4)某溶液中含有Al3+,为提纯Al3+可以控制溶液的pH范围为______________。
(5)从图中选取适当的数据计算Al(OH)3的溶度积(Ksp)=________________
(6)用石墨电极电解AlCl3溶液,试写出电解初始阶段的化学方程式:______________。
(1)C(s)+H2O(g)=CO(g)+H2(g) △H= +131kJ/mol
(2)CO-2e-+4OH-=CO32-+2H2O
(3)Al3++3NH3·H2O=Al(OH)3↓+3NH4+;Al(OH)3+OH-=[Al(OH)4]-(写成Al(OH)3+OH-= AlO2-+2H2O也可以)
(4)5~8
(5)10-32
(4)2AlCl3+6H2O 2Al(OH)3↓+3H2↑+3Cl2↑
2Al(OH)3↓+3H2↑+3Cl2↑
(2)CO-2e-+4OH-=CO32-+2H2O
(3)Al3++3NH3·H2O=Al(OH)3↓+3NH4+;Al(OH)3+OH-=[Al(OH)4]-(写成Al(OH)3+OH-= AlO2-+2H2O也可以)
(4)5~8
(5)10-32
(4)2AlCl3+6H2O
 2Al(OH)3↓+3H2↑+3Cl2↑
2Al(OH)3↓+3H2↑+3Cl2↑ 
练习册系列答案
相关题目




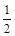 O2(g)=H2O(g);△H2=-241.8kJ·mol-1
O2(g)=H2O(g);△H2=-241.8kJ·mol-1