题目内容
12.有机物A、B、C、D、E之间发生如下的转化: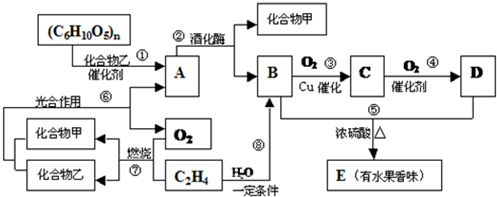
(1)写出D分子中官能团的名称:羧基,C物质的结构简式:CH3CHO.
(2)上述①~⑧转化反应中,属于取代反应的有⑤;属于加成反应的有⑧.(用反应序号填写)
(3)向A的水溶液中加入新制的Cu(OH)2并加热时产生的实验现象是有(砖)红色沉淀产生.
(4)请写出下列转化的化学反应方程式:
①(C6H10O5)n→A:(C6H10O5)n+nH2O$→_{△}^{催化剂}$nC6H12O6; ②B+D→E:CH3CH2OH+CH3COOH$?_{△}^{催化剂}$CH3COOC2H5+H2O;③乙烯生成聚乙烯:nCH2═CH2$\stackrel{催化剂}{→}$
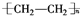 .
.
分析 根据题中各物质转化关系,反应⑥是光合作用产生A和氧气,则A为葡萄糖(C6H12O6),(C6H10O5)n水解能产生葡萄糖,所化合物乙为水,反应①为糖类的水解,反应②葡萄糖在酒化酶的作用生成化合物甲为二氧化碳,B为CH3CH2OH,反应③为B发生氧化反应生成C为CH3CHO,反应④为C发生氧化反应生成D为CH3COOH,反应⑤为B和D发生酯化反应生成E为CH3COOC2H5,反应⑦为乙烯的燃烧反应生成二氧化碳和水,反应⑧为乙烯与水加成生成乙醇,据此答题.
解答 解:根据题中各物质转化关系,反应⑥是光合作用产生A和氧气,则A为葡萄糖(C6H12O6),(C6H10O5)n水解能产生葡萄糖,所化合物乙为水,反应①为糖类的水解,反应②葡萄糖在酒化酶的作用生成化合物甲为二氧化碳,B为CH3CH2OH,反应③为B发生氧化反应生成C为CH3CHO,反应④为C发生氧化反应生成D为CH3COOH,反应⑤为B和D发生酯化反应生成E为CH3COOC2H5,反应⑦为乙烯的燃烧反应生成二氧化碳和水,反应⑧为乙烯与水加成生成乙醇,
(1)D为CH3COOH,D分子中官能团的名称为羧基,C为CH3CHO,
故答案为:羧基;CH3CHO;
(2)根据上面的分析可知,上述①~⑧转化反应中,属于取代反应的有 ⑤;属于加成反应的有⑧,
故答案为:⑤;⑧;
(3)A为葡萄糖(C6H12O6),向A的水溶液中加入新制的Cu(OH)2并加热时产生的实验现象是有(砖)红色沉淀产生,
故答案为:有(砖)红色沉淀产生;
(4)请写出下列转化的化学反应方程式:
①(C6H10O5)n→A的化学反应方程式为(C6H10O5)n+nH2O$→_{△}^{催化剂}$ nC6H12O6,②B+D→E的化学反应方程式为CH3CH2OH+CH3COOH$?_{△}^{催化剂}$CH3COOC2H5+H2O,③乙烯生成聚乙烯的化学反应方程式为nCH2═CH2 $\stackrel{催化剂}{→}$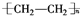 ,
,
故答案为:(C6H10O5)n+nH2O$→_{△}^{催化剂}$ nC6H12O6;CH3CH2OH+CH3COOH$?_{△}^{催化剂}$CH3COOC2H5+H2O;nCH2═CH2 $\stackrel{催化剂}{→}$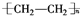 .
.
点评 本题考查有机物推断,涉及烯烃、醇、醛、羧酸性质与转化,关键是确定C的结构简式,再根据转化关系推断,难度不大,注意对基础知识的理解掌握.

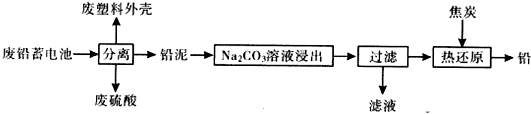
部分难溶电解质的性质如表:
| 物质 | Ksp(25℃) | 颜色 |
| PbSO4 | 1.8×10-8 | 白色 |
| PbCO3 | 1.5×10-13 | 白色 |
| PbCrO4 | 1.8×10-14 | 黄色 |
| BaCrO4 | 1.2×10-10 | 黄色 |
| Pb(OH)2 | 1.4×10-20 | 白色 |
(1)废铅蓄电池需回收处理的原因是金属资源的回收(或铅等重金属会引起污染、酸污染等)(回答一点)
(2)将废硫酸和滤液合并后可提取一种钠盐副产品(相对分子质量为322),已知副产品带10个结晶水的结晶水合物,则其化学式Na2SO4•10H2O,由滤液提取该副产品的主要实验步骤依次为蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(3)利用铅泥中的PbSO4溶于CH3COONa溶液生成可溶于水的(CH3COO)2Pb,(CH3COO)2Pb溶液与KClO在强碱性条件下反应制取PbO2,写出后一步生成PbO2的离子方程式CH3COO)2Pb+ClO-+2OH-=Pb02↓+Cl-+2CH3COO-+H2O.
(4)25℃时,Na2CO3溶液浸出时发生反应为:CO32-(aq)+PbSO4(s)?PbCO3(s)+SO42-(aq).测得滤液中c(CO32-)=1×10-5mol/L计算c(SO42-)=1.2mol/L
(5)滤渣PbCO3和焦炭共热可制得金属铅,写出该化学方程式2PbCO3+C$\frac{\underline{\;\;△\;\;}}{\;}$2Pb+3CO2(或PbCO3+2C$\frac{\underline{\;\;△\;\;}}{\;}$Pb+3CO)
(6)已知Pb(OH)2是既能溶于稀硝酸,又能溶于KOH溶液的两性氢氧化物.利用题目所给信息,设计实验区别PbCrO4和BaCrO4:取少量待测物于两支试管中,分别与过量KOH溶液反应,能溶解的是PbCr04,不溶解的是BaCr04.
| A. | 乙炔 | B. | 甲苯 | C. | 苯 | D. | 乙烯 |
| A. | 升高温度 | B. | 加入生成物 | ||
| C. | 缩小容器体积 | D. | 增加反应物的物质的量 |
| A. | 容器中CO2、H2、CH3OH、H2O的物质的量之比为1:3:1:1 | |
| B. | v正(CO2)=v逆(H2O) | |
| C. | 容器内混合气体密度保持不变 | |
| D. | 3molH-H键断裂同时断裂3molH-O键 |
| A. | 0.1 mol氮气中所含的氮原子数是0.1NA | |
| B. | 标准状况下,2.24 L乙醇中所含的分子数是0.1NA | |
| C. | 1mol•L-1 氨水溶液中含NH4+的数目是NA | |
| D. | 24g镁和足量的盐酸反应,电子转移的数目是2NA |
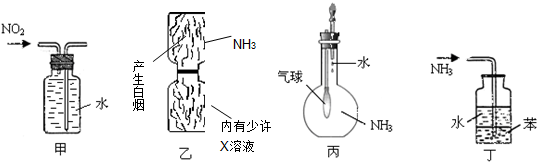
| A. | 图甲:收集NO2气体 | B. | 图乙:验证X溶液为浓硫酸 | ||
| C. | 图丙:验证氨气在水中的溶解性 | D. | 图丁:用于吸收尾气NH3 |
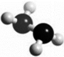 肼(N2H4)是火箭燃料,常温下为液体,其分子的球棍模型如图所示.肼能与双氧水发生反应:N2H4+2H2O2═N2+4H2O.下列说法正确的是( )
肼(N2H4)是火箭燃料,常温下为液体,其分子的球棍模型如图所示.肼能与双氧水发生反应:N2H4+2H2O2═N2+4H2O.下列说法正确的是( )| A. | 标准状况下,11.2L N2H4中含共用电子对数为2.5NA | |
| B. | 1mol N2H4和1mol H2O2含有的电子总数不相等 | |
| C. | 若生成3.6g H2O,则上述反应转移电子的数目为0.2 NA | |
| D. | N2H4和H2O2均只含有极性共价键 |