题目内容
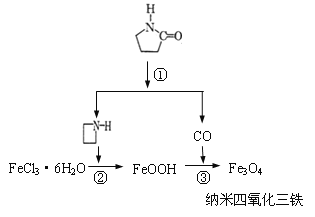
【题目】纳米Fe3O4晶体材料可以作为核磁共振造影增强剂,用于疾病的诊断和治疗。其制备过程如图所示、下列叙述不合理的是
A.在反应②中,![]() 的作用可能是促进氯化铁水解
的作用可能是促进氯化铁水解
B.反应③的化学方程式是:6FeOOH + CO ==2Fe3O4+3H2O+CO2
C.直接加热FeCl3溶液也可以得到四氧化三铁
D.纳米四氧化三铁形成的分散剂,有可能产生丁达尔现象
【答案】C
【解析】
试题分析:A、因反应②环丙胺不参加反应,但加快反应速率,即加快了氯化铁水解,故A合理;B、由制备过程图可知,反应③的反应物为FeOOH和CO,由一种生成物为Fe3O4和质量守恒定律可知反应为6FeOOH+CO═2Fe3O4+3H2O+CO2,故B合理;C、直接加热FeCl3溶液可以得到氢氧化铁,进一步加热可以得到氧化铁,得不到四氧化三铁,故C不合理;D、纳米四氧化三铁分散在适当分散剂中,属于胶体分散系,则具有丁达尔现象,故D正确;故选C。

【题目】某化学活动小组设计如图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质. 
(1)装置A中发生反应的离子方程式为 .
(2)该实验装置明显存在不足之处,改进的措施为
(3)已知在装置C中通入一定量的氯气后,观察到测得D中有黄红色的气体(提示:是一种氯的氧化物).已知C中所得固体含有NaHCO3 . 现对C中的成分进行猜想和探究. ①提出合理假设.
假设一:存在两种成分,为NaHCO3、NaCl
假设二:存在三种成分,为NaHCO3、Na2CO3、NaCl
②设计方案并实验.请在表格中写出实验步骤以及预期现象和结论.
限选试剂和仪器:蒸馏水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、试管、小烧杯.
步骤 | 预期现象和结论 |
步骤1:取C中少量样品于试管中,滴加足量蒸馏水 | 固体物质全部完全溶解 |
步骤:向A试管中滴加适量BaCl溶液 | a. 如果 |
步骤: | 有白色沉淀生成,C的部分有NaCl |
结论:由步骤3的结论结合步骤2中的a,则假设一成立;由步骤3的结论结合步骤2中的b,则假设二成立.
若C中有0.1molCl2恰好与10.6gNa2CO3反应,且假设一成立,由此可推知C中反应生成的氯的氧化物为(写化学式),写出C中发生反应的化学方程式 .
【题目】下列图中的实验方案,能达到实验目的的是
A | B | C | D | |
实验方案 |
将NO2球浸泡在冰水热水中 |
|
|
|
实验目的 | 探究温度对平衡 2NO2 | 验证FeCl3对H2O2分解反应有催化作用 | 除去CO2气体中混有的SO2 | 比较HCl、H2CO3和H2SiO3的酸性强弱 |
A. A B. B C. C D. D






