题目内容
11.NA为阿伏伽德罗常数的值.下列说法正确的是( )| A. | 标准状况下,2.24 L NO2溶于水完全反应转移电子数为0.2NA | |
| B. | 标准状况下,5.6L二氧化碳气体中含有的氧原子数为0.5NA | |
| C. | 氢原子数为0.6NA的乙烯分子中含有的π键数为0.2NA | |
| D. | 0.1L0.5mol/LCH3COOH溶液中含有的氢离子数为0.05NA |
分析 A、求出二氧化氮的物质的量,然后根据3mol二氧化氮和水反应转移2mol电子来分析;
B、NO2气体中存在平衡:2NO2?N2O4;
C、1mol乙烯中含4molH原子,含1molπ键;
D、醋酸是弱电解质.
解答 解:A、标况下2.24L二氧化氮的物质的量为0.1mol,而3mol二氧化氮和水反应转移2mol电子,故0.1mol二氧化氮和水完全反应转移电子数为$\frac{0.1mol}{3}×2$=$\frac{2}{30}$mol电子,即$\frac{2}{30}$NA个,故A错误;
B、标况下5.6L二氧化碳气体的物质的量为0.25mol,故含有的氧原子个数为0.5NA个,故B正确;
C、1个乙烯分子中含4个H原子,含1个π键,故氢原子数为0.6NA的乙烯分子的个数为0.15NA个,则含有的π键个数为0.15NA个,故C错误;
D、醋酸是弱电解质,不能完全电离,故溶液中的氢离子个数小于0.05NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
19.下列叙述正确的是( )
| A. | 铝粉与氧化镁共热可制取金属镁 | |
| B. | 铝分别与足量的 HCl溶液、足量的NaOH的溶液反应,产生的氢气前者多 | |
| C. | 氯化汞(HgCl2)的稀溶液可用于手术器械消毒,因为它会使蛋白质变性,杀菌消毒 | |
| D. | NaOH溶液可以盛装在带玻璃塞的磨口试剂瓶中 |
16.某溶液中存在Mg2+、Ag+、Ba2+三种金属离子,现用NaOH、Na2CO3、NaCl三种溶液使它们分别沉淀并分离出,要求每次只加一种溶液,滤出一种沉淀,所加溶液顺序正确的是( )
| A. | Na2CO3 NaCl NaOH | B. | NaOH NaCl Na2CO3 | ||
| C. | NaCl NaOH Na2CO3 | D. | NaCl Na2CO3 NaOH |
20.下列表示物质结构的化学用语正确的是( )
| A. | 8个中子的碳原子的核素符号:12C | B. | HF的电子式: | ||
| C. | 氯化镁  | D. | Cl-离子的结构示意图: |
1.下列操作或装置能达到实验目的是( )
| A. |  检验铁粉与水蒸气反应产生的氢气 | |
| B. |  快速制备和收集一定量的氨气 | |
| C. |  分离互溶但沸点相差较大的液体混合物 | |
| D. | 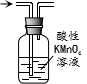 除去甲烷中少量的乙烯得纯净甲烷 |


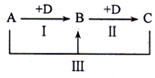 A、B、C、D表示中学化学中的四种常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去).
A、B、C、D表示中学化学中的四种常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去).