题目内容
 在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:
在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:2MnO4-+5C2O42-+16H+
| ||
8H2O.
(1)若用托盘天平称取W g Na2C2O4晶体,称量开始时和称量结束时的共同操作步骤是
(2)若将W g Na2C2O4配成100mL标准溶液,移取20.00mL置于锥形瓶中,则酸性KMnO4溶液应装在
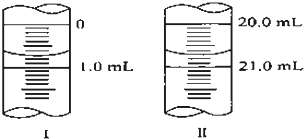
(3)若滴定管的起始读数和终点读数如图所示,则所取标准溶液的体积为
(4)下列实验操作会对滴定结果产生的后果(填“偏高”、“偏低”或“无影响”):
①观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果
②若将锥形瓶用标准液润洗,则滴定结果
考点:中和滴定
专题:实验题
分析:(1)称量固体时,无论开始时,还是称量结束时,都需移动游码;
(2)高锰酸钾具有强氧化性,能腐蚀碱式滴定管的橡皮管;KMnO4溶液呈紫色,草酸反应完毕,滴入最后一滴KMnO4溶液,溶液由无色变为浅紫红色,且半分钟不褪色为滴定到终点;
(3)根据滴定管的结构、精确度以及测量原理来解答;根据关系式KMnO4~5Na2C2O4来计算;
(4)根据c(待测)=
分析不当操作对V(待测)的影响,以此判断浓度的误差.
(2)高锰酸钾具有强氧化性,能腐蚀碱式滴定管的橡皮管;KMnO4溶液呈紫色,草酸反应完毕,滴入最后一滴KMnO4溶液,溶液由无色变为浅紫红色,且半分钟不褪色为滴定到终点;
(3)根据滴定管的结构、精确度以及测量原理来解答;根据关系式KMnO4~5Na2C2O4来计算;
(4)根据c(待测)=
| V(标准)×c(标准) |
| V(待测) |
解答:
解:(1)若用托盘天平称取W g Na2C2O4晶体,称量开始时和称量结束时的共同操作步骤是移动游码,使游码回零处;
故答案为:把游码拨回零处;
(2)高锰酸钾具有强氧化性,能腐蚀碱式滴定管的橡皮管,应装在酸式滴定管中;KMnO4溶液呈紫色,草酸反应完毕,滴入最后一滴KMnO4溶液,溶液由无色变为浅紫红色,且半分钟不褪色为滴定到终点,
故答案为:酸式;滴入最后一滴KMnO4溶液,溶液由无色变为浅紫红色,且半分钟不褪色;
(3)滴定管的起始读数为0.70mL,终点读数为20.70mL,酸性KMnO4溶液消耗的体积为20.70mL-0.70mL=20.00mL;
KMnO4溶液的物质的量浓度为c,WgNa2C2O4配成100mL标准溶液,20.00mL溶液中含有Na2C2O4的质量为
g;
2KMnO4 ~5Na2C2O4
2moL 5×134g
0.02L×c
g
解得:c=
mol?L-1,
故答案为:22.00;
mol?L-1;
(4)①观察酸式滴定管液面时,开始俯视,滴定终点平视,造成V(待测)偏大,据c(待测)=
分析,则滴定结果偏小;
②若将锥形瓶用标准液润洗,标准液的物质的量偏多,造成V(待测)偏大,据c(待测)=
分析,则滴定结果偏小;
故答案为:偏小;偏小;
故答案为:把游码拨回零处;
(2)高锰酸钾具有强氧化性,能腐蚀碱式滴定管的橡皮管,应装在酸式滴定管中;KMnO4溶液呈紫色,草酸反应完毕,滴入最后一滴KMnO4溶液,溶液由无色变为浅紫红色,且半分钟不褪色为滴定到终点,
故答案为:酸式;滴入最后一滴KMnO4溶液,溶液由无色变为浅紫红色,且半分钟不褪色;
(3)滴定管的起始读数为0.70mL,终点读数为20.70mL,酸性KMnO4溶液消耗的体积为20.70mL-0.70mL=20.00mL;
KMnO4溶液的物质的量浓度为c,WgNa2C2O4配成100mL标准溶液,20.00mL溶液中含有Na2C2O4的质量为
| W |
| 5 |
2KMnO4 ~5Na2C2O4
2moL 5×134g
0.02L×c
| W |
| 5 |
解得:c=
| 2W |
| 67 |
故答案为:22.00;
| 2W |
| 67 |
(4)①观察酸式滴定管液面时,开始俯视,滴定终点平视,造成V(待测)偏大,据c(待测)=
| V(标准)×c(标准) |
| V(待测) |
②若将锥形瓶用标准液润洗,标准液的物质的量偏多,造成V(待测)偏大,据c(待测)=
| V(标准)×c(标准) |
| V(待测) |
故答案为:偏小;偏小;
点评:本题是一道氧化还原反应滴定的综合题,涉及天平的使用、中和滴定的注意事项和化学计算,注意该题为待测液滴定标准液,考查了学生分析问题和解决问题的能力.

练习册系列答案
相关题目
X、Y、Z、M为4种短周期元素,X、Y位于同周期且原子半径r(X)>r(Y),Y2-与M+的电子层结构相同,X与Z的原子核外最外层电子数相同,Z的单质可制成半导体材料.下列说法不正确的是( )
| A、单质M的晶体是体心立方堆积,M的配位数是8 |
| B、XY2、ZY2、M2Y的晶体分别属于3种不同类型的晶体 |
| C、X的氢化物X2H2分子中含有2个σ键和2个π键 |
| D、由元素X与Z形成的化合物中只含共价键 |
中学化学实验室经常用到下列实验装置,其中不可用于物质分离的装置是( )
A、 |
B、 |
C、 |
D、 |
化学与生产、生活密切相关,下列说法正确的是( )
| A、BaSO4在医学上用做钡餐,是因为Ba2+没有毒 |
| B、FeCl3溶液能与Cu反应,可用于蚀刻印刷电路 |
| C、14C可用于文物的年代鉴定,14C与12C互为同分异构体 |
| D、NO2在光照下能使O2经过复杂的反应生成O3,所以氮氧化物不会破坏臭氧层 |