题目内容
3.下表中给出几种氯化物的熔点和沸点:| NaCl | MgCl2 | AlCl3 | SiCl4 | |
| 熔点(℃) | 801 | 714 | 190 | -70 |
| 沸点(℃) | 1413 | 1412 | 180 | 57.57 |
| A. | ①② | B. | ②③ | C. | ①②③ | D. | ②③④ |
分析 根据表格中氯化物的熔沸点判断物质的晶体类型,一般离子晶体的熔沸点大于分子晶体的熔沸点.
解答 解:①由表格中的数据可知AlCl3的熔沸点较低,则AlCl3属于分子晶体,加热时能升华,故①正确;
②由表格中的数据可知SiCl4的熔沸点较低,则SiCl4是分子晶体,故②正确;
③由表格中的数据可知,NaCl的沸点为1465℃,则属于离子晶体,粒子之间以离子键结合,故③错误;
④由表格中的数据可知AlCl3的熔沸点较低,则AlCl3属于分子晶体,故④错误;
故选A.
点评 本题考查晶体类型与晶体熔沸点的关系,明确表格中的数据及一般离子晶体的熔沸点大于分子晶体的熔沸点是解答本题的关键,难度不大.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
14.X、Y、Z是原子序数依次递增的短周期元素,3种元素的原子核外电子数之和与Ca2+的核外电子数相等,X、Z分别得到一个电子后均形成稀有气体原子的稳定电子层结构.下列说法正确的是( )
| A. | Z与X形成化合物的沸点高于Z的同族元素与X形成化合物的沸点 | |
| B. | 原子半径:Z>Y>X | |
| C. | CaY2与水发生氧化还原反应时,CaY2只作氧化剂 | |
| D. | CaY2和CaZ22种化合物中,阳离子与阴离子个数比均为1:2 |
11.下列有关硝酸化学性质的叙述中,正确的是( )
| A. | 浓、稀硝酸都能使蓝色石蕊试纸最终变为红色 | |
| B. | 硝酸能与Cu反应,只表现氧化性 | |
| C. | 硝酸可与Na2S反应制得H2S气体 | |
| D. | 浓硝酸因分解放出的NO2又溶解于硝酸而呈黄色 |
18.下列说法中正确的是( )
| A. | 乙烷和氯气按1:1混合,在光照下发生取代反应时,有机产物只有一种 | |
| B. | 在氧气中燃烧时只生成CO2和H2O的物质一定是烃 | |
| C. | 乙酸是有机弱酸,所以它的酸性比碳酸弱 | |
| D. | 在酯化反应中,羧酸脱去羧基中的羟基,醇脱去羟基中的氢而生成酯 |
8.页岩气是蕴藏于页岩层中的天然气,我州页岩气蕴藏量达4.81万亿立方米,约占全省近7成,可采储量超过1.443万亿立方米.页岩气将是我州能源开发的重要方向.下列有关结论中错误的是( )
| A. | 页岩气是一种清洁的能源 | |
| B. | 使用页岩气是对化学能的充分利用 | |
| C. | 使用页岩气给农民的生活带来了不便 | |
| D. | 页岩气是我州解决能源的重要途径 |
15.随着手机、手提电脑、数码相机等电器的普及,锂电池的生产量和消费量大.造成资源短缺,钴的毒性又很大.因此,回收锂电池既有较大的经济价值,又有益于保护生态环境.某课题小组提出如下方案对某钴酸锂正极材料(主要含LiCoO2、铝箔、性质稳定的导电剂等)进行回收钴等金属.
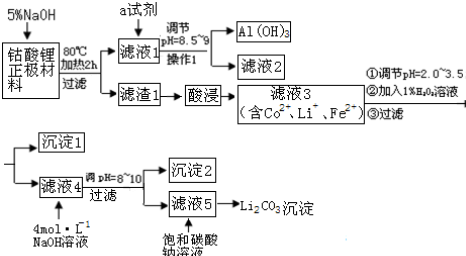
已知:金属氢氧化物沉淀的pH值
回答下列问题:
(1)写出钴酸锂正极材料用加5%氢氧化钠溶液,发生的离子反应方程式2Al+2OH-+2H2O=2AlO2-+3H2↑
(2)操作1所用到的玻璃仪器除烧杯、漏斗外,还必须有玻璃棒(填仪器名称).
(3)滤液4到沉淀2可以选择抽滤,抽滤不仅能加快过滤速度,而且能得到比较干燥的晶体.但是,太细的晶体不适合于抽滤.一般情况下,下列哪些因素有利于得到较大的晶体AC.(填写序号)
A.缓慢冷却溶液B.溶质溶解度较小
C.缓慢蒸发溶剂 D.溶液浓度较高
(4)该课题组同学将滤渣1酸浸溶解得到Co2+用盐酸进行溶解.发生如下反应:
2LiCoO2+8HCl═2CoCl2+Cl2+2LiCl+4H2O
在此反应中,体现了盐酸的酸性和还原性.
指导老师建议采用稀硫酸和H2O2溶液溶解,发生如下反应:
2LiCoO2+□+6H++1H2O2=2Co2++1O2↑+2Li++4□
在上述方程式的□中填上缺少的微粒,并进行配平.
你认为指导老师提出该建议的主要依据是用盐酸溶解会产生有毒的氯气污染环境,同时为了除去溶液的Fe2+,还要再加H2O2,操作麻烦
(5)试剂a最好选用下列试剂中的C
A.NaOH溶液 B.(NH4)2CO3溶液 C.NH4HCO3
(6)沉淀2的化学式是Co(OH)2.

已知:金属氢氧化物沉淀的pH值
| 金属氢氧化物 | 金属离子浓度 1mol•L-1 | 金属离子浓度 0.1mol•L-1 | 沉淀完全时的pH值 | |
| 分子式 | Ksp | 开始沉淀时的pH | ||
| Fe(OH)2 | 4.87×10-17 | 5.8 | 6.3 | 8.3 |
| Fe(OH)3 | 2.79×10-39 | 1.2 | 1.5 | 2.8 |
| Co(OH)2 | 5.92×10-15 | 6.9 | 7.4 | 9.4 |
(1)写出钴酸锂正极材料用加5%氢氧化钠溶液,发生的离子反应方程式2Al+2OH-+2H2O=2AlO2-+3H2↑
(2)操作1所用到的玻璃仪器除烧杯、漏斗外,还必须有玻璃棒(填仪器名称).
(3)滤液4到沉淀2可以选择抽滤,抽滤不仅能加快过滤速度,而且能得到比较干燥的晶体.但是,太细的晶体不适合于抽滤.一般情况下,下列哪些因素有利于得到较大的晶体AC.(填写序号)
A.缓慢冷却溶液B.溶质溶解度较小
C.缓慢蒸发溶剂 D.溶液浓度较高
(4)该课题组同学将滤渣1酸浸溶解得到Co2+用盐酸进行溶解.发生如下反应:
2LiCoO2+8HCl═2CoCl2+Cl2+2LiCl+4H2O
在此反应中,体现了盐酸的酸性和还原性.
指导老师建议采用稀硫酸和H2O2溶液溶解,发生如下反应:
2LiCoO2+□+6H++1H2O2=2Co2++1O2↑+2Li++4□
在上述方程式的□中填上缺少的微粒,并进行配平.
你认为指导老师提出该建议的主要依据是用盐酸溶解会产生有毒的氯气污染环境,同时为了除去溶液的Fe2+,还要再加H2O2,操作麻烦
(5)试剂a最好选用下列试剂中的C
A.NaOH溶液 B.(NH4)2CO3溶液 C.NH4HCO3
(6)沉淀2的化学式是Co(OH)2.
12.同温同压下,将一定量的硫化氢和二氧化硫混合后恰好完全反应,若反应中转移的电子是1mol,则在反应中生成的硫为( )
| A. | 1 mol | B. | 0.75 mol | C. | 0.5 mol | D. | 0.25 mol |
13.甲、乙两同学用如图所示装置进行实验,探究硝酸与铁反应的产物.
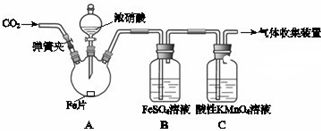
文献记载:
I.在浓硝酸和活泼金属反应过程中,随着硝酸浓度的降低,其生成的产物有+4、+2、-3价等氮的化合物.
II.FeSO4+NO?Fe(NO)SO4(棕色)△H<0.
III.NO2和NO都能被KMnO4氧化吸收.
甲的实验操作和现象记录如下:
请回答下列问题:
(1)滴入浓硝酸加热前没有明显现象的原因是常温时,铁遇浓硝酸形成致密氧化膜,阻止反应进一步发生.
(2)检验是否生成-3价氮的化合物,应进行的实验操作是取少量反应后A中溶液于试管中,向其中加入浓NaOH溶液,加热,用湿润的红色石蕊试纸接近试管口.若试纸变蓝,则A中生成NH4+.
(3)证明A溶液中是否含有Fe3+,选择的药品是(填序号)d
a.铁粉 b.溴水 c.铁氰化钾溶液 d.硫氰化钾溶液.
(4)根据实验现象写出A中一定发生反应的化学方程式Fe+4HNO3(浓)=Fe(NO3)2+2NO2↑+2H2O.

文献记载:
I.在浓硝酸和活泼金属反应过程中,随着硝酸浓度的降低,其生成的产物有+4、+2、-3价等氮的化合物.
II.FeSO4+NO?Fe(NO)SO4(棕色)△H<0.
III.NO2和NO都能被KMnO4氧化吸收.
甲的实验操作和现象记录如下:
| 实验操作 | 实验现象 |
| 打开弹簧夹,通入一段时间CO2,关闭弹簧夹. | |
| 打开分液漏斗活塞,将浓硝酸缓慢滴入烧瓶中,关闭活塞. | 无明显现象. |
| 加热烧瓶,反应开始后停止加热. | ①A中有红棕色气体产生,一段时间后,B中溶液变棕色; C中溶液紫色变浅. ②反应停止后,A中无固体剩余. |
(1)滴入浓硝酸加热前没有明显现象的原因是常温时,铁遇浓硝酸形成致密氧化膜,阻止反应进一步发生.
(2)检验是否生成-3价氮的化合物,应进行的实验操作是取少量反应后A中溶液于试管中,向其中加入浓NaOH溶液,加热,用湿润的红色石蕊试纸接近试管口.若试纸变蓝,则A中生成NH4+.
(3)证明A溶液中是否含有Fe3+,选择的药品是(填序号)d
a.铁粉 b.溴水 c.铁氰化钾溶液 d.硫氰化钾溶液.
(4)根据实验现象写出A中一定发生反应的化学方程式Fe+4HNO3(浓)=Fe(NO3)2+2NO2↑+2H2O.
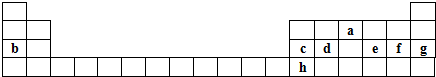
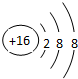 .
.