题目内容
下列说法中正确的是( )
| A、原电池中的电极一定要由两种不同的金属组成 |
| B、原电池中电子流出的一极是正极,发生氧化反应 |
| C、原电池两极均发生氧化还原反应 |
| D、原电池中阳离子向正极移动 |
考点:原电池和电解池的工作原理
专题:
分析:A.原电池中的电极可能由导电的非金属和金属组成;
B.原电池中电子流出的电极是负极,发生氧化反应;
C.原电池负极发生氧化反应、正极发生还原反应;
D.原电池放电时,电解质中阳离子向正极移动、阴离子向负极移动.
B.原电池中电子流出的电极是负极,发生氧化反应;
C.原电池负极发生氧化反应、正极发生还原反应;
D.原电池放电时,电解质中阳离子向正极移动、阴离子向负极移动.
解答:
解:A.原电池中的电极可能由导电的非金属和金属组成,如Zn、石墨和稀硫酸构成的原电池,故A错误;
B.原电池中电子流出的电极是负极,发生氧化反应,电子流入的电极是正极,发生还原反应,故B错误;
C.原电池负极失电子发生氧化反应、正极得电子发生还原反应,故C错误;
D.原电池放电时,电解质中阳离子向正极移动、阴离子向负极移动,从而形成内电路,故D正确;
故选D.
B.原电池中电子流出的电极是负极,发生氧化反应,电子流入的电极是正极,发生还原反应,故B错误;
C.原电池负极失电子发生氧化反应、正极得电子发生还原反应,故C错误;
D.原电池放电时,电解质中阳离子向正极移动、阴离子向负极移动,从而形成内电路,故D正确;
故选D.
点评:本题考查原电池原理,知道正负极的反应、判断方法、离子移动方向,注意原电池中电极不一定是金属,如燃料电池中电极材料为石墨,易错选项是D.

练习册系列答案
相关题目
设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、等质量的N2和CO所含分子数均为NA |
| B、1 mol?L-1NaCl溶液含有Cl-的个数为NA |
| C、常温常压下48gO2和48gO3含有的氧原子数均为3NA |
| D、标准状况下,22.4 L水中含有NA个H2O分子 |
在下列反应中,水作还原剂的是( )
| A、CaO+H2O=Ca(OH)2 |
| B、2Na+2H2O=2NaOH+H2↑ |
| C、2F2+2H2O=4HF+O2 |
| D、HCl+NaOH=NaCl+H2O |
可逆反应A+B(s)?C达到平衡后,无论加压或降温,A的转化率都增大,则下列结论正确的是( )
| A、A为固体,C为气体,正反应为放热反应 |
| B、A为气体,C为固体,正反应为吸热反应 |
| C、A为气体,C为固体,正反应为放热反应 |
| D、A、C均为气体,正反应为吸热反应 |
X元素原子的质量数为m,核内中子数为n,则Wg X2+离子含有的电子的物质的量约为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
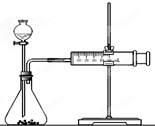 影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.