题目内容
6.图为某化学反应速率-时间图.在t1时刻升高温度或增大压强,都符合下图所示变化的反应是( )
| A. | 2SO2(g)+O2(g)?2SO3(g);△H<0 | B. | 4NH3(g)+O2(g)?4NO(g)+6H2O (g);△H<0 | ||
| C. | H2(g)+I2(g)?2HI (g);△H>0 | D. | C (s)+H2O (g)?CO (g)+H2 (g);△H>0 |
分析 根据图知,升高温度或增大压强时,逆反应速率大于正反应速率,则平衡逆向移动,说明逆反应是吸热反应、反应前后气体计量数之和增大,据此分析解答.
解答 解:根据图知,升高温度或增大压强时,逆反应速率大于正反应速率,则平衡逆向移动,升高温度平衡向吸热方向移动、增大压强平衡向气体体积减小方向移动,所以该图象说明逆反应是吸热反应、反应前后气体计量数之和增大,符合条件的为B,故选B.
点评 本题考查图象分析,为高频考点,明确压强、温度对化学平衡影响原理及v-t图象是解本题关键,会根据图象判断移动方向,题目难度不大.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
16.离子是构成物质的基本微粒之一,下表中是中学常见的离子:
回答下列问题:
(1)Cl-离子的结构示意图是 . Al3+、K+、SO42-三种离子可组成一种盐,写出该盐的一种用途净水剂.
. Al3+、K+、SO42-三种离子可组成一种盐,写出该盐的一种用途净水剂.
(2)将含OH-离子的溶液 滴入浓度均为0.1 mol/L的Al3+和NH4+的混合溶液中,若测得溶液中NH4+减少了一半,此时,溶液中不存在(填“存在”或“不存在”)大量的Al3+.
(3)物质A和B分别由上表中的两种离子组成,将它们分别溶于水中,A的溶液显酸性,将A、B两溶液混合,微热,既有白色沉淀,又有使湿润的红色石蕊试纸变蓝的气体生成.
则B的阳离子是Ba2+,用离子方程式表示A溶液显酸性的原因NH4++H2O NH3•H2O+H+.
NH3•H2O+H+.
(4)常温下,将(NH4)2CO3溶于水,得到含有大量NH4+和CO32-的溶液,往溶液中滴入少量氨水,测得溶液中N H4+和CO32 -的浓度比为2:1,此时该溶液的pH<( 填“<”、“=”或“>”)7.
(5)在微生物作用的条件下,NH4+可被空气氧化成NO3-.写出该反应的离子方程式:NH4++2O2=NO3-+H2O+2H+.
(6)在一个固定容积为5L的密闭容器中充入0.10mol N2和0.30molH2,一定条件下,半分钟后达到平衡,测得容器中含NH3 0.08mol,则ν(H2)=0.048mol.L-1.min-1,此时N2的转化率为40%;若继续通入0.10mol N2和0.30molH2,则平衡向正反应方向移动(填“向正反应方向”、“向逆反应方向”或“不”).
| 阳离子 | K+、Al3+、Ba2+、NH4+ |
| 阴离子 | Cl-、OH-、SO42-、CO32- |
(1)Cl-离子的结构示意图是
 . Al3+、K+、SO42-三种离子可组成一种盐,写出该盐的一种用途净水剂.
. Al3+、K+、SO42-三种离子可组成一种盐,写出该盐的一种用途净水剂.(2)将含OH-离子的溶液 滴入浓度均为0.1 mol/L的Al3+和NH4+的混合溶液中,若测得溶液中NH4+减少了一半,此时,溶液中不存在(填“存在”或“不存在”)大量的Al3+.
(3)物质A和B分别由上表中的两种离子组成,将它们分别溶于水中,A的溶液显酸性,将A、B两溶液混合,微热,既有白色沉淀,又有使湿润的红色石蕊试纸变蓝的气体生成.
则B的阳离子是Ba2+,用离子方程式表示A溶液显酸性的原因NH4++H2O
 NH3•H2O+H+.
NH3•H2O+H+.(4)常温下,将(NH4)2CO3溶于水,得到含有大量NH4+和CO32-的溶液,往溶液中滴入少量氨水,测得溶液中N H4+和CO32 -的浓度比为2:1,此时该溶液的pH<( 填“<”、“=”或“>”)7.
(5)在微生物作用的条件下,NH4+可被空气氧化成NO3-.写出该反应的离子方程式:NH4++2O2=NO3-+H2O+2H+.
(6)在一个固定容积为5L的密闭容器中充入0.10mol N2和0.30molH2,一定条件下,半分钟后达到平衡,测得容器中含NH3 0.08mol,则ν(H2)=0.048mol.L-1.min-1,此时N2的转化率为40%;若继续通入0.10mol N2和0.30molH2,则平衡向正反应方向移动(填“向正反应方向”、“向逆反应方向”或“不”).
17.氢气在氯气中燃烧时产生苍白色火焰.在反应过程中,破坏2mol氯气中的化学键消耗的能量为Q1kJ,破坏2mol氢气中的化学键消耗的能量为Q2kJ,形成4mol氯化氢的化学键释放的能量为Q3kJ.下列关系式中正确的是( )
| A. | Q1+Q2>Q3 | B. | Q1+Q2>2Q3 | C. | Q1+Q2<Q3 | D. | Q1+Q2=Q3 |
11.生活中的一些问题常涉及到化学知识,则下列叙述正确的是( )
| A. | 氢氧化铁溶胶、水玻璃、淀粉溶液、PM2.5微粒均具有丁达尔效应 | |
| B. | 明矾和漂白粉常用于自来水的处理,两者的作用原理相同 | |
| C. | 氯化铁溶液可用于制作印刷电路板是因为其具有较强氧化性,与铜发生置换反应 | |
| D. | 高温能杀死流感病毒是因为构成病毒的蛋白质受热变性 |
15.下列物质属于碱的是( )
| A. | 纯碱 | B. | 碱式碳酸铜 | C. | 漂白粉 | D. | 烧碱 |
16.下列化学用语正确的是( )
| A. | 14C原子的结构示意图: | |
| B. | H2O2的电子式: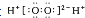 | |
| C. | NH4C的电子式: | |
| D. | 原子核内有10个中子的氧原子${\;}_{8}^{16}$O |