题目内容
100℃时,0.01mol·L-1 NaHSO4溶液中水电离的c(H+) =10-10 mol·L-1,将pH=8的Ba(OH)2溶液V1L与pH=5,V2 L NaHSO4混合(忽略溶液体积变化),所得溶液pH=7,则V1:V2=( )
A.1:9 B.1:1 C.2:9 D.1:2
【答案】
C
【解析】
试题分析:硫酸氢钠溶液中水电离出的氢离子浓度等于溶液中氢氧根离子浓度,0.01mol·L-1 NaHSO4溶液中C(H+)=0.01mol·L-1,水电离的c(H+)=c(OH-)=10-10 mol·L-1,所以Kw=10-12;该温度下,氢氧化钡溶液中c(OH-)=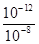 mol·L-1=10-4 mol·L-1,混合溶液呈碱性,溶液中c(OH-)=
mol·L-1=10-4 mol·L-1,混合溶液呈碱性,溶液中c(OH-)=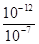 mol·L-1=10-5 mol·L-1,
mol·L-1=10-5 mol·L-1,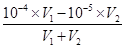 =10-5,所以V1:V2=2:9,选C.
=10-5,所以V1:V2=2:9,选C.
考点:酸碱混合时的定性判断及有关pH的计算

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
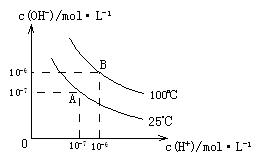
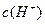 和
和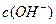 的关系如下图所示:
的关系如下图所示: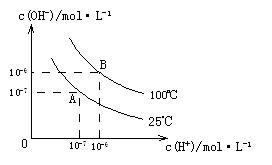
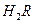 在水溶液中的电离方程式为:
在水溶液中的电离方程式为: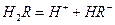 ,
,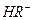

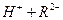 。
。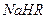 溶液中,各离子浓度由大到小的顺序是:
溶液中,各离子浓度由大到小的顺序是: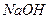 溶液的pH = 。
溶液的pH = 。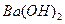 溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则
溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则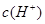 和
和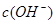 的关系如下图所示:
的关系如下图所示: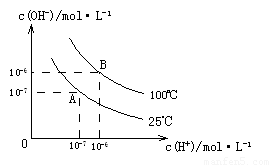
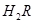 在水溶液中的电离方程式为:
在水溶液中的电离方程式为: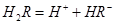 ,
,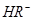
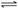
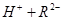 。
。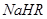 溶液中,各离子浓度由大到小的顺序是:
溶液中,各离子浓度由大到小的顺序是: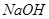 溶液的pH = 。
溶液的pH = 。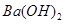 溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则
溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则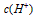 和
和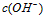 的关系如下图所示
的关系如下图所示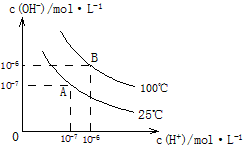
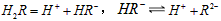 。
。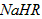 溶液中,各离子浓度由大到小的顺序是:_____________________。
溶液中,各离子浓度由大到小的顺序是:_____________________。 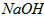 溶液的pH =_________________。
溶液的pH =_________________。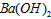 溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH=
溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH=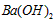 溶液与盐酸的体积比为____________________。
溶液与盐酸的体积比为____________________。