题目内容
10.实验室中配制AgNO3溶液时通常需要向其中加入硝酸目的是抑制Ag+水解;AgCl在水中存在沉淀溶解平衡:AgCl(s)?Ag+(aq)+Cl-(aq).25℃时,现将足量AgCl分别放入:①100mL蒸馏水;②100mL 0.2mol•L-1AgNO3溶液;③100mL 0.1mol•L-1氯化镁溶液;④100mL 0.1mol•L-1氯化钠溶液.充分搅拌后,相同温度下Ag+浓度由大到小的顺序是②①④③ (填写序号).分析 AgNO3为强酸弱碱盐,水解显酸性,加酸抑制水解;对AgCl(s)?Ag+(aq)+Cl-(aq),加硝酸银时Ag+浓度增大,加含氯离子的物质,溶解平衡逆向移动,以此来解答.
解答 解:实验室中配制AgNO3溶液时通常需要向其中加入硝酸目的是抑制Ag+水解;对AgCl(s)?Ag+(aq)+Cl-(aq),②加硝酸银,Ag+浓度最大,①③④相比,氯离子浓度为①<④<③,含氯离子的物质,溶解平衡逆向移动,银离子浓度减小,则相同温度下Ag+浓度由大到小的顺序是②①④③,
故答案为:抑制Ag+水解;②①④③.
点评 本题考查难溶电解质的溶解平衡,为高频考点,把握水解平衡、难溶电解质的溶解平衡移动为解答的关键,侧重分析与应用能力的考查,注意平衡移动原理的应用,题目难度不大.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
1.把4mol A气体和4mol B气体混合放入2L的恒容密闭容器中,在一定条件下发生反应:2A(g)+2B(g)?C(g)+2D(g);经5min达到平衡,测得压强减小了10%,下列说法中正确的是( )
| A. | 平衡体系中C的体积分数为$\frac{1}{9}$ | B. | 平衡时A的浓度为2.4mol/L | ||
| C. | D的平均速率为0.32mol/L•min | D. | B的转化率为20% |
18.A、B、C、D、E是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如表:
请回答下列问题(用对应元素的元素符号作答):
(1)写出D元素基态原子的价电子排布式3s23p1,E2+价电子的轨道表示式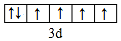 .
.
(2)这5种元素中电负性最大的元素是O(填元素符号),A、B、C三种元素的第一电离能由大到小的顺序为N>O>C(填元素符号)
(3)B、C、D的简单离子的半径由大到小的顺序为N3->O2->Al3+(用离子符号表示)
(4)写出C的核外有18个电子的氢化物的电子式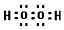 .
.
| 元素 | 相关信息 |
| A | 基态原子的价电子排布式为nSnnPn |
| B | 基态原子中的未成对电子数是同周期中最多的 |
| C | 最外层电子数是电子层数的3倍 |
| D | 简单离子是第三周期元素中离子半径最小的 |
| E | 价电子层中的未成对电子数为4 |
(1)写出D元素基态原子的价电子排布式3s23p1,E2+价电子的轨道表示式
 .
.(2)这5种元素中电负性最大的元素是O(填元素符号),A、B、C三种元素的第一电离能由大到小的顺序为N>O>C(填元素符号)
(3)B、C、D的简单离子的半径由大到小的顺序为N3->O2->Al3+(用离子符号表示)
(4)写出C的核外有18个电子的氢化物的电子式
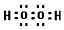 .
.
5.常温下,下列有关0.1mol•L-1的NH4Cl溶液的说法正确的是( )
| A. | pH相同的盐酸与氯化铵溶液中,水的电离程度相同 | |
| B. | 溶液加水稀释时,$\frac{c(N{H}_{3}{H}_{2}O)•c({H}^{+})}{c(N{H}_{4}^{+})}$逐渐增大 | |
| C. | 加入少量Mg(OH)2固体,c(NH4+)减小 | |
| D. | 加入等体积0.05mol﹒L-1NaOH溶液时:c(Na+)=c(CI-)>c(NH4+)>c(OH-)>c(H+) |
15. 如图所示,将两烧杯中电极用导线相连,四个电极分别为Mg、Al、Pt、C.当闭合开关S后,以下表述正确的是( )
如图所示,将两烧杯中电极用导线相连,四个电极分别为Mg、Al、Pt、C.当闭合开关S后,以下表述正确的是( )
 如图所示,将两烧杯中电极用导线相连,四个电极分别为Mg、Al、Pt、C.当闭合开关S后,以下表述正确的是( )
如图所示,将两烧杯中电极用导线相连,四个电极分别为Mg、Al、Pt、C.当闭合开关S后,以下表述正确的是( )| A. | 电流表指针不发生偏转 | |
| B. | Al、Pt两极有H2产生 | |
| C. | 甲池pH增大,乙池pH减小 | |
| D. | Mg、C两极生成的气体在一定条件下可以恰好完全反应 |
2.下列说法正确的是( )
| A. | 水溶液中能电离出H+的化合物叫做酸 | |
| B. | 实验测得2mol某气体体积为44.8L,则测定条件一定是标准状况 | |
| C. | 摩尔是七个基本物理量之一 | |
| D. | 化合物分为酸、碱、盐和氧化物是用树状分类法分类的 |
19.烯烃、炔烃因含不饱和键能被酸性KMnO4溶液氧化,下列各物质中不属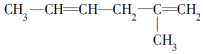 被酸性高锰酸钾氧化的产物的是( )
被酸性高锰酸钾氧化的产物的是( )
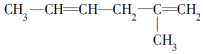 被酸性高锰酸钾氧化的产物的是( )
被酸性高锰酸钾氧化的产物的是( )| A. | CO2 | B. | CH3COOH | ||
| C. | 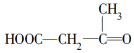 | D. | HOOC-CH2-CH2-COOH |
20.在给定条件下,下列选项所示的物质间转化均能实现的是( )
| A. | SiO2$\stackrel{HCl(aq)}{→}$SiCl4$\frac{{H}_{2}}{高温}$Si | |
| B. | MgCO3$\stackrel{HCl(aq)}{→}$MgCl2(aq)$\stackrel{电解}{→}$Mg | |
| C. | N2$→_{高温、高压、催化剂}^{H_{2}}$NH${\;}_{{\;}_{3}}$$\stackrel{HCl(aq)}{→}$NH4Cl(aq) | |
| D. | FeS$\stackrel{HCl(aq)}{→}$H2S$→_{煅烧}^{O_{2}}$SO2$→_{点燃}^{氧气}$H2SO4 |