题目内容
4.用NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 2.4g镁变成Mg2+时失去的电子数目为0.2NA | |
| B. | 常温常压下,11.2L氧气所含的O原子数为NA | |
| C. | 如果11.2LN2中含有n个分子,则阿伏加德罗常数一定为2n | |
| D. | 1 mol•L-1的KSCN和1mol•L-1KAl(SO4)2溶液中,所含K+数都是NA |
分析 A.根据n=$\frac{m}{M}$计算出镁的物质的量,然后计算出失去电子的物质的量及数目;
B.常温常压下,不能使用标况下的气体摩尔体积计算;
C.不是标况下,无法计算氮气的物质的量;
D.缺少溶液体积,无法计算含有钾离子数目.
解答 解:A.2.4g镁的物质的量为:$\frac{2.4g}{24g/mol}$=0.1mol,变成0.1mol Mg2+时失去0.2mol电子,失去电子的数目为0.2NA,故A正确;
B.不是标况下,不能使用标准状况下的气体摩尔体积计算,故B错误;
C.不是标准状况下,不能使用标况下的气体摩尔体积计算11.2LN2的物质的量,故C错误;
D.没有告诉1 mol•L-1的KSCN和1mol•L-1KAl(SO4)2溶液的体积,无法计算溶液中含有钾离子的数目,故D错误;
故选A.
点评 本题考查阿伏加德罗常数的有应用,题目难度中等,注意明确标况下气体摩尔体积的使用条件,掌握以物质的量为中心的各化学量与阿伏加德罗常数的关系,试题侧重考查学生的分析能力及化学计算能力.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
13.当光束通过下列分散系时,可能产生丁达尔效应的是( )
| A. | NaCl溶液 | B. | 蒸馏水 | C. | 盐酸 | D. | 稀豆浆 |
15.下列仪器名称正确的是( )
| A. | 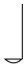 钥匙 | B. |  蒸发皿 | C. | 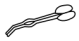 镊子 | D. |  滴瓶 |
19.下列常见现象与胶体无关的是( )
| A. | 清晨在密林中看到一缕缕的光束 | |
| B. | FeCl3溶液加入NaOH溶液产生红褐色沉淀 | |
| C. | 利用电泳将油漆、乳胶、橡胶等微粒均匀地沉积在镀件上 | |
| D. | 向豆浆中加入硫酸钙使蛋白质等聚沉,制成可口的豆腐 |
16.下列溶液中,SO42-的物质的量浓度最大的是( )
| A. | 7.5 mL 2 mol•L-1KAl(SO4)2溶液 | B. | 30 mL 1 mol•L-1 MgSO4溶液 | ||
| C. | 20 mL 0.5 mol•L-1Al2(SO4)3溶液 | D. | 10 mL 3 mol•L-1 Na2SO4溶液 |
13.0.1mol/L CH3COONa溶液中,下列关系正确的是( )
| A. | c(H+)=c(OH-) | B. | c(CH3COOH)+c(CH3COO-)=0.1 mol/L | ||
| C. | c(CH3COOH)>c(CH3COO-) | D. | c(H+)>c(OH-) |
14.下列化学用语正确的是( )
| A. | 甲烷的电子式: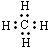 | |
| B. | 氟原子的结构示意图: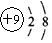 | |
| C. | 乙烯的结构简式:CH2CH2 | |
| D. | 碳酸钠的电离方程式:Na2CO3=Na2++CO32- |