题目内容
17.铅蓄电池的总反应式为:PbO2+Pb+2H2SO4$?_{充电}^{放电}$2PbSO4+2H2O据此判断下列叙述正确的是( )| A. | 放电时,H2SO4浓度增加 | |
| B. | 放电时,负极的电极反应式为:Pb+SO42--2e-═PbSO4 | |
| C. | 在充电时,电池中每转移1 mol电子,理论上生成2 mol硫酸 | |
| D. | 在充电时,阴极发生的反应是PbSO4-2e-+2H2O═PbO2+SO42-+4H+ |
分析 A.根据电池反应式确定硫酸浓度是否变化;
B.原电池负极上失电子发生氧化反应;
C.根据充电的总反应分析,每生成1molPb,则转移2mol电子,同时也生成2mol硫酸,据此分析;
D.充电时,负极与阴极相连得电子发生还原反应.
解答 解:A.根据电池反应式知,放电时消耗硫酸,所以硫酸浓度降低,故A错误;
B.蓄电池放电时,负极上铅失电子和硫酸根离子反应生成硫酸铅,电极反应式为:Pb+SO42--2e-=PbSO4,故B正确;
C.由充电的总反应分析,每生成1molPb,则转移2mol电子,同时也生成2mol硫酸,所以电池中每转移1mol电子,理论上生成1mol硫酸,故C错误;
D.充电时,负极与阴极相连,则阴极的电极反应为PbSO4+2e-=Pb+SO42-,故D错误;
故选B.
点评 本题考查铅蓄电池,注意原电池和电解池的分析,明确工作原理及电子守恒是解答本题的关键,题目难度中等.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
8.在下列元素中,不属于主族元素的是( )
| A. | p | B. | Fe | C. | Ca | D. | I |
5.下列用电子式表示化合物的形成过程正确的是( )
| A. |  | B. | 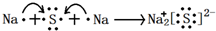 | ||
| C. |  | D. | 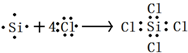 |
2.下列物质的水溶液经加热浓缩,蒸干灼烧仍能得到原物质的是( )
| A. | FeCl3 | B. | Na2CO3 | C. | Na2SO3 | D. | Cu(NO3)2 |
9.如表是元素周期表的一部分,请回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为 .
.
(2)表中能形成两性氢氧化物的元素是Al(用元素符号表示),写出该元素的单质与⑨最高价氧化物对应水化物反应的化学方程式2Al+2KOH+2H2O═2KAlO2+3H2↑.
(3)元素⑥、⑦氢化物的稳定性顺序为HCl>H2S (填写化学式);
(4)设计实验方案:比较⑦与⑩单质氧化性的强弱,请将方案填入如表.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .
.(2)表中能形成两性氢氧化物的元素是Al(用元素符号表示),写出该元素的单质与⑨最高价氧化物对应水化物反应的化学方程式2Al+2KOH+2H2O═2KAlO2+3H2↑.
(3)元素⑥、⑦氢化物的稳定性顺序为HCl>H2S (填写化学式);
(4)设计实验方案:比较⑦与⑩单质氧化性的强弱,请将方案填入如表.
| 实验步骤 | 实验现象 | 结论与化学反应方程式 |
6.如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22.下列说法正确的是( )
| X | Y | ||
| W | Z | ||
| T |
| A. | X、Y、Z三种元素最低价氢化物的沸点依次升高 | |
| B. | T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 | |
| C. | 由X、Y和氢三种元素形成的化合物中只有共价键 | |
| D. | 物质WY2、W3X4、WZ4均有熔点高、硬度小的特性 |
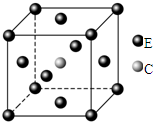 原子序数依次递增且都小于36的A、B、C、D、E五种元素,其中A的一种核素中没有中子,B原子基态时最外层电子数是其内层电子数的2倍,D原子基态时2p原子轨道上有2个未成对的电子,E元素的原子结构中3d能级上未成对电子数是成对电子数的2倍.回答下列问题:
原子序数依次递增且都小于36的A、B、C、D、E五种元素,其中A的一种核素中没有中子,B原子基态时最外层电子数是其内层电子数的2倍,D原子基态时2p原子轨道上有2个未成对的电子,E元素的原子结构中3d能级上未成对电子数是成对电子数的2倍.回答下列问题: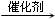
 .
.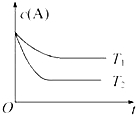 反应A(g)?B(g)+C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol•L-1.温度T1和T2下A的浓度与时间关系如图所示.回答下列问题:
反应A(g)?B(g)+C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol•L-1.温度T1和T2下A的浓度与时间关系如图所示.回答下列问题: