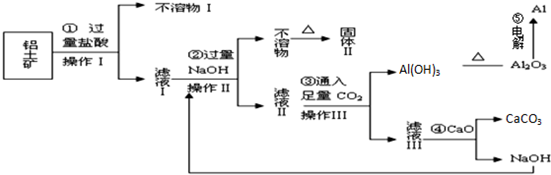
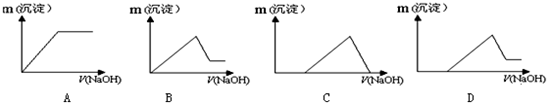
题目内容
下表为元素周期表的一部分,其中编号代表对应的元素.
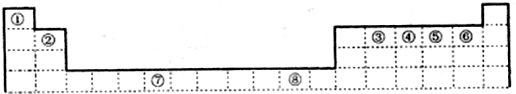
请回答下列问题:
(1)写出元素⑦的基态原子外围电子排布式 ,元素⑧位于 区.⑤元素原子的价层电子的轨道表示式为 ,
(2)若元素①③⑤形成的某化合物显酸性,经测定这三种元素的质量比为1:6:16,该化合物对氢气的相对密度为23,则其中所有杂化原子的杂化方式分别为 和 .
(3)元素③④⑤⑥的第一电离能由大到小的顺序是 (用元素符号表示).请写出由④和⑤两种元素形成的与N3ˉ互为等电子体的分子的化学式 ,(写出一种即可)其VSEPR构型为 .

请回答下列问题:
(1)写出元素⑦的基态原子外围电子排布式
(2)若元素①③⑤形成的某化合物显酸性,经测定这三种元素的质量比为1:6:16,该化合物对氢气的相对密度为23,则其中所有杂化原子的杂化方式分别为
(3)元素③④⑤⑥的第一电离能由大到小的顺序是
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:根据元素在周期表中的位置知,①②③④⑤⑥⑦⑧分别是H、Be、C、N、O、F、Cr、Cu元素,
(1)元素⑦的基态原子外围电子为3d、4s电子,根据构造原理书写其外围电子排布式,根据最后填入电子名称确定区域名称,⑤是O元素,其2S、2P电子为其原子价电子;
(2)若元素①③⑤形成的某化合物显酸性,经测定这三种元素的质量比为1:6:16,则这三种元素的原子个数之比=
:
:
=2:1:2,该化合物对氢气的相对密度为23,则该化合物的相对分子质量为46,所以分子式为CH2O2,为HCOOH,根据价层电子对互斥理论确定原子杂化类型;
(3)同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第VA族元素第一电离能大于相邻元素;
由④和⑤两种元素形成的与N3ˉ互为等电子体的分子是N2O,根据价层电子对互斥理论确定其VSEPR构型.
(1)元素⑦的基态原子外围电子为3d、4s电子,根据构造原理书写其外围电子排布式,根据最后填入电子名称确定区域名称,⑤是O元素,其2S、2P电子为其原子价电子;
(2)若元素①③⑤形成的某化合物显酸性,经测定这三种元素的质量比为1:6:16,则这三种元素的原子个数之比=
| 1 |
| 1 |
| 6 |
| 12 |
| 16 |
| 16 |
(3)同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第VA族元素第一电离能大于相邻元素;
由④和⑤两种元素形成的与N3ˉ互为等电子体的分子是N2O,根据价层电子对互斥理论确定其VSEPR构型.
解答:
解:根据元素在周期表中的位置知,①②③④⑤⑥⑦⑧分别是H、Be、C、N、O、F、Cr、Cu元素,
(1)元素⑦的基态原子外围电子为3d、4s电子,根据构造原理书知其外围电子排布式为3d54s1,该元素位于ds区,⑤是O元素,其2S、2P电子为其原子价电子,则⑤元素原子的价层电子的轨道表示式为 ,
,
故答案为:3d54s1;ds; ;
;
(2)若元素①③⑤形成的某化合物显酸性,经测定这三种元素的质量比为1:6:16,则这三种元素的原子个数之比=
:
:
=2:1:2,该化合物对氢气的相对密度为23,则该化合物的相对分子质量为46,所以分子式为CH2O2,为HCOOH,C原子和羰基上O原子都含有3个σ键,所以为sp2杂化,羟基上O原子含有2个σ键和2个孤电子对,所以为sp3杂化,故答案为:sp2;sp3;
(3)同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第VA族元素第一电离能大于相邻元素,所以③④⑤⑥的第一电离能由大到小的顺序为F>N>O>C,
由④和⑤两种元素形成的与N3ˉ互为等电子体的分子是N2O,该分子中价层电子对个数=2+
×(6-2×3)=2,所以为直线形分子,故答案为:F>N>O>C;N2O;直线形.
(1)元素⑦的基态原子外围电子为3d、4s电子,根据构造原理书知其外围电子排布式为3d54s1,该元素位于ds区,⑤是O元素,其2S、2P电子为其原子价电子,则⑤元素原子的价层电子的轨道表示式为
 ,
,故答案为:3d54s1;ds;
 ;
;(2)若元素①③⑤形成的某化合物显酸性,经测定这三种元素的质量比为1:6:16,则这三种元素的原子个数之比=
| 1 |
| 1 |
| 6 |
| 12 |
| 16 |
| 16 |
(3)同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第VA族元素第一电离能大于相邻元素,所以③④⑤⑥的第一电离能由大到小的顺序为F>N>O>C,
由④和⑤两种元素形成的与N3ˉ互为等电子体的分子是N2O,该分子中价层电子对个数=2+
| 1 |
| 2 |
点评:本题考查了元素周期表和元素周期律的综合应用,涉及原子杂化方式的判断、微粒空间构型的判断等知识点,根据价层电子对互斥理论、原子结构等知识点来分析解答,注意第一电离能规律中的异常现象,为易错点.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
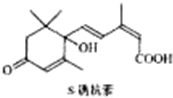 对盆栽鲜花施用S-诱抗素制剂,可以保持鲜花盛开.S-诱抗素的分子结构如图,则1mol该物质与足量的NaOH溶液反应时最多可消耗NaOH的物质的量为( )
对盆栽鲜花施用S-诱抗素制剂,可以保持鲜花盛开.S-诱抗素的分子结构如图,则1mol该物质与足量的NaOH溶液反应时最多可消耗NaOH的物质的量为( )| A、1mol | B、2mol |
| C、3mol | D、4mol |
常温下,pH=12的NaOH溶液和pH=2的醋酸混合后恰好完全反应(不考虑溶液体积的变化).下列说法正确的是( )
| A、反应后的溶液呈酸性 |
| B、两种反应物中水电离出的c(H+)都是1×10-12mol?L-1 |
| C、反应后的溶液中:c(CH3COO-)+c(CH3COOH)═0.01mol?L-1 |
| D、反应后的溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
能达到实验目的是( )
A、 称NaOH固体的质量 |
B、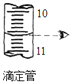 读数为10.60 |
C、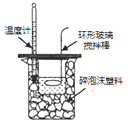 反应热的测定 |
D、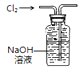 收集氯气 |
已知X、Y、Z、W四种短周期元素在周期表中的相对位置如图所示,下列说法不正确的是( )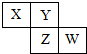
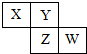
| A、Z元素的原子半径比Y元素的大 |
| B、若Y的最低化合价为-2,则W的最高正化合价为+6 |
| C、若Z的最高正化合价为+5,则X元素的化合物最多 |
| D、若HmZOn为强酸,则Y是活泼非金属元素 |