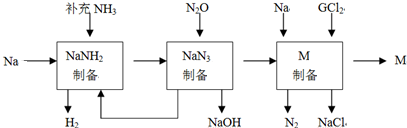
��Ŀ����
8��R��X��Y��Z������Ԫ�أ����ڳ����������л��ϼ۾�Ϊ+2�ۣ���X2+�뵥��R����Ӧ�� X2++Z�TX+Z2+��Y+Z2+=Y2++Z�����������ӱ���ԭ��0��ʱ���ֵ������Դ�С���ϣ�������| A�� | X2+��R2+��Y2+��Z2+ | B�� | Y2+��Z2+��R2+��X2+ | C�� | Z2+��X2+��R2+��Y2+ | D�� | R2+��X2+��Z2+��Y2+ |
���� �Է����е�������ԭ��Ӧ�У��������������Դ�����������������ԣ��ݴ˷������
��� �⣺�Է����е�������ԭ��Ӧ�У��������������Դ�����������������ԣ�R��X��Y��Z����Ԫ�أ����dz����Ļ��ϼ۾�Ϊ+2�ۣ�X2++Z�TX+Z2+��X2+����������Z2+���������������X2+��Z2+��Y+Z2+�TY2++Z����������Z2+������������Y2+��������Z2+��Y2+��X2+�뵥��R����Ӧ��������R2+��Z2+��
����������ǿ��˳����R2+��X2+��Z2+��Y2+��
��ѡD��
���� ���⿼��������ǿ���жϣ���ȷ�����ԡ���ԭ��ǿ���ȽϷ����ǽⱾ��ؼ���֪������Ԫ�ػ��ϼۣ���Ŀ�ѶȲ���

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
19������������Ҵ����ڱ��ӡ�����ȩ���ܱ�ϩ�ᣨCH2=CHCOOH����������������������ˮ������KMnO4��Һ��NaHCO3��Һ���ܷ�Ӧ���ǣ�������
| A�� | �٢� | B�� | �ڢ� | C�� | �� | D�� | �ۢ� |
16����������������Ӧ�ö�Ӧ��ϵ��ȷ���ǣ�������
| A�� | �������л�ԭ�ԣ������ڼ��HClй© | |
| B�� | Ũ���������ˮ�ԣ������ڸ���CO2 | |
| C�� | ���������и��۵㣬�����������ͻ�ש | |
| D�� | Cl2�����ԣ������ռӦ�Ʊ����������� |
3������˵������ȷ���ǣ�������
| A�� | ����Ӿ��е��������ǻ�� | |
| B�� | ����Ӧ��Ũ�ȣ����������ӵİٷ������Ӷ�ʹ��Ч��ײ�������� | |
| C�� | ���������ȷ�Ӧ���Ƿ��ȷ�Ӧ�������¶ȶ����������Ӱٷ��� | |
| D�� | ����Ӽ����ײһ������Ч��ײ |
13�������йػ�ѧ����������ȷ���ǣ�������
| A�� | �Ҵ��ķ���ʽC2H5OH | B�� | �����ӵĽṹʾ��ͼ��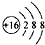 | ||
| C�� | NH4Cl�ĵ���ʽ��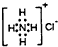 | D�� | ���ȼױ��Ľṹ��ʽ��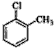 |
20�������[Ag��NH3��2]OH�У������ڵĻ�ѧ���ǣ�������
| A�� | ���Ӽ� | B�� | ������ | C�� | ��� | D�� | ��λ�� |
18�����н�����ʵ�Ļ�ѧ����ʽ�����ӷ���ʽ����ȷ���ǣ�������
| A�� | ��AgCl����Һ�м���KI��Һ��AgCl��s��+I-��aq���TAgI��s��+Cl-��aq�� | |
| B�� | ������ˮ��Al3++3H2O?Al��OH��3+3H+ | |
| C�� | 90��ʱ����ô�ˮ��Kw=3.8��10-13��H2O��l��?H+��aq��+OH-��aq����H��0 | |
| D�� | ���ȵĴ�����Һ������ϴ���ۣ�CO32-+H2O?HCO3-+OH- |