题目内容
常温下,CaSO4在水中的沉淀溶解平衡曲线如图所示,已知 Ksp(CaSO4)=9×10-6。下列说法正确的是( )


| A.a点对应的KSP小于c点对应的KSP |
| B.a点变为b点将有沉淀生成 |
| C.加入蒸馏水可以使c点变为d点 |
D.含有大量 的溶液中肯定不存在Ca2+ 的溶液中肯定不存在Ca2+ |
B
试题分析:A、Ksp是一常数,温度不变Ksp不变,在曲线上的任意一点Ksp都相等,故A错误;
B、硫酸钙溶液中存在着溶解平衡,a点在平衡曲线上增大c(SO42-),平衡左移,将有沉淀生成,故B正确;
C、d点时溶液不饱和,蒸发溶剂水,c(SO42-)、c(Ba2+)均增大,故C错误;
D、硫酸钙溶液中存在着溶解平衡, SO42-、Ba2+溶液中都有,故D错误。
故选B。
点评:本题考查沉淀溶解平衡,题目难度中等,注意理解难溶电解质在水中的沉淀溶解平衡特点,正确理解和掌握溶度积KSP的概念。

练习册系列答案
相关题目
 。若某氢氧化镁溶液的PH=9,则该溶液中c(Mg2+)最大为
。若某氢氧化镁溶液的PH=9,则该溶液中c(Mg2+)最大为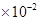 mol/L
mol/L  mol/L
mol/L
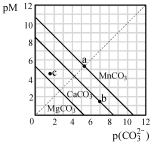
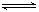 cC(g)+dD(g)达到平衡时,各物质的物质的量浓度满足以下关系:
cC(g)+dD(g)达到平衡时,各物质的物质的量浓度满足以下关系: (为一常数),K称为化学平衡常数,它的值只与温度有关。现有反应:CO(g)+H2O(g)
(为一常数),K称为化学平衡常数,它的值只与温度有关。现有反应:CO(g)+H2O(g)