题目内容
下表是元素周期表的一部分,针对表中的①~⑥元素,回答下列问题
(1)最活泼的金属元素是 (填元素符号)
(2)最活泼的非金属元素单质是 (写化学式)
(3)②和⑥两种元素原子半径较大的是 (填元素符号)
(4)⑤和⑥两种元素最高价氧化物对应的水合物为碱的是 (填元素符号);
(5)写出①的单质在③的单质中燃烧的化学方程式 .
| 主族 周期 | ⅠA | 0族 | ||||||
| 一 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 二 | ② | ③ | ||||||
| 三 | ④ | ⑤ | ⑥ | |||||
(2)最活泼的非金属元素单质是
(3)②和⑥两种元素原子半径较大的是
(4)⑤和⑥两种元素最高价氧化物对应的水合物为碱的是
(5)写出①的单质在③的单质中燃烧的化学方程式
考点:位置结构性质的相互关系应用,元素周期律和元素周期表的综合应用
专题:
分析:由元素在周期表中位置,可知①为H、②为C、③为O、④为Na、⑤为Mg、⑥为Si.
(1)同周期自左而右金属性减弱,同主族自上而下金属性增强;
(2)同周期自左而右非金属性增强,同主族自上而下非金属性减弱;
(3)同主族从上到下原子半径增大;
(4)Mg为金属,Si为非金属;
(5)①的单质在③的单质中燃烧生成水.
(1)同周期自左而右金属性减弱,同主族自上而下金属性增强;
(2)同周期自左而右非金属性增强,同主族自上而下非金属性减弱;
(3)同主族从上到下原子半径增大;
(4)Mg为金属,Si为非金属;
(5)①的单质在③的单质中燃烧生成水.
解答:
解:由元素在周期表中位置,可知①为H、②为C、③为O、④为Na、⑤为Mg、⑥为Si.
(1)同周期自左而右金属性减弱,同主族自上而下金属性增强,则上述元素中最活泼金属元素为Na,故答案为:Na;
(2)同周期自左而右非金属性增强,同主族自上而下非金属性减弱,上述元素中最活泼的非金属元素单质是O2,故答案为:O2;
(3)同主族从上到下原子半径增大,则②和⑥两种元素原子半径较大的是Si,故答案为:Si;
(4)Mg为金属,Si为非金属,则⑤和⑥两种元素最高价氧化物对应的水合物为碱的是Mg,故答案为:Mg;
(5)①的单质在③的单质中燃烧生成水,方程式为O2+2H2
2H2O,故答案为:O2+2H2
2H2O.
(1)同周期自左而右金属性减弱,同主族自上而下金属性增强,则上述元素中最活泼金属元素为Na,故答案为:Na;
(2)同周期自左而右非金属性增强,同主族自上而下非金属性减弱,上述元素中最活泼的非金属元素单质是O2,故答案为:O2;
(3)同主族从上到下原子半径增大,则②和⑥两种元素原子半径较大的是Si,故答案为:Si;
(4)Mg为金属,Si为非金属,则⑤和⑥两种元素最高价氧化物对应的水合物为碱的是Mg,故答案为:Mg;
(5)①的单质在③的单质中燃烧生成水,方程式为O2+2H2
| ||
| ||
点评:本题考查位置、结构性质的关系及应用,为高频考点,涉及元素周期表与元素周期律的理解及应用,题目难度不大,注意把握金属性、非金属性及原子半径比较.

练习册系列答案
相关题目
在指定环境中,下列各组离子一定可以大量共存的是( )
| A、使甲基橙变红的溶液中:Cr2O72-、Fe2+、SO42-、K+ |
| B、无色强酸性溶液中:Na+、Cl-、SO42-、[Cu(NH3)4]2+ |
| C、加入过量氨水溶液仍然澄清的溶液中:Cu2+、Ag+、NO3-、NH4+ |
| D、能使碘化钾淀粉试纸变蓝的溶液中:Na+、NH4+、S2-、Br- |
铝不易被腐蚀,其主要原因是( )
| A、铝是一种轻金属 |
| B、铝的金属活动性比镁弱 |
| C、铝具有较高熔点 |
| D、铝易形成致密的氧化物薄膜 |
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1),下列说法错误的是( )
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
| NH3的平衡浓度(mol?L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | a1 | a2 | a3 |
| A、2c1<c3 |
| B、a+b=92.4 |
| C、a1+a3<1 |
| D、p3>2p2=2p1 |
下列家庭化学小实验不能达到预期目的是( )
| A、食醋(含CH3COOH)可以用来洗涤热水瓶胆中的污垢[含CaCO3、Mg(OH)2] |
| B、用鸡蛋白、食盐、水完成蛋白质的溶解、盐析实验 |
| C、用米汤检验食用加碘盐(含KIO3)中含有碘 |
| D、用灼烧方法鉴别纯毛线和棉布 |
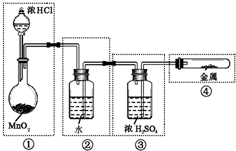 实验室用MnO2与浓HCl反应制Cl2,若用如图所示的实验装置来制备纯净、干燥的氯气,并试验它与金属镁粉的反应.每个虚线框表示一个单元装置,其中错误的是( )
实验室用MnO2与浓HCl反应制Cl2,若用如图所示的实验装置来制备纯净、干燥的氯气,并试验它与金属镁粉的反应.每个虚线框表示一个单元装置,其中错误的是( )| A、只有①和②处 |
| B、只有②处 |
| C、只有①、②和③处 |
| D、①、②、③、④处 |
下列有关平衡常数(K、Ka、Kw)的说法中错误的是( )
| A、各平衡常数的大小与温度有关 |
| B、若温度升高则各平衡常数一定增大 |
| C、平衡常数的大小能说明反应(或电离、溶解)进行的程度 |
| D、平衡常数越大反应(或电离)程度越大 |
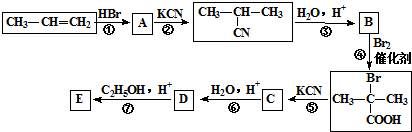
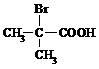 与足量NaOH溶液反应的化学方程式为
与足量NaOH溶液反应的化学方程式为