题目内容
标准状况下,将6.72L乙烯和乙炔的混合气体通入足量的溴水中,溴水质量增加了8g,求混合气体中乙烯和乙炔的体积分数,以及反应了的溴的质量.
考点:有关混合物反应的计算
专题:计算题
分析:乙烯、乙炔都与溴水发生加成反应,溴水质量增加了8g为乙烯、乙炔的总质量,再结合二者总体积列方程计算各自物质的量,进而计算混合气体中乙烯和乙炔的体积分数;根据乙烯、乙炔的物质的量计算参加反应溴的物质的量,进而计算参加反应的溴的质量.
解答:
解:标准状况下,6.72L乙烯和乙炔的混合气体的总物质的量为
=0.3mol,乙烯、乙炔都与溴水发生加成反应,溴水质量增加了8g为乙烯、乙炔的总质量,
令乙烯、乙炔的物质的量分别为xmol、ymol,则:
解得x=0.1 y=0.2
故乙烯的体积分数为
×100%=33.3%,乙炔的体积分数=1-33.3%=66.7%,
参加反应溴的物质的量为:0.1mol+0.2mol×2=0.5mol,故参加反应溴的质量为0.5mol×160g/mol=80g,
答:乙烯的体积分数33.3%,乙炔的体积分数66.7%,反应溴的质量为80g.
| 6.72L |
| 22.4L/mol |
令乙烯、乙炔的物质的量分别为xmol、ymol,则:
|
解得x=0.1 y=0.2
故乙烯的体积分数为
| 0.1mol |
| 0.1mol+0.3mol |
参加反应溴的物质的量为:0.1mol+0.2mol×2=0.5mol,故参加反应溴的质量为0.5mol×160g/mol=80g,
答:乙烯的体积分数33.3%,乙炔的体积分数66.7%,反应溴的质量为80g.
点评:本题考查混合物计算、加成反应等,难度不大,侧重对基础知识的巩固.

练习册系列答案
相关题目
下列说法正确的是( )
| A、用洁净的Pt蘸取某溶液进行焰色反应,火焰呈黄色;该溶液中一定含有Na+,无k+ |
| B、用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧; CO2、H2O与Na2O2反应是放热反应 |
| C、向溴水中滴入植物油,振荡后,油层显无色; 溴不溶于油脂 |
| D、将硫酸酸化的H2O2滴入Fe(NO3)2溶液,溶液变黄色; H2O2的氧化性比Fe3+强 |
镁、铝、铁合金投入到300ml硝酸溶液中,金属恰好溶解,转化成Mg2+、Al3+和Fe3+;硝酸全部被还原为NO,且在标准状况下,体积为6.72L,当加入300ml某浓度NaOH,金属阳离子恰好全部沉淀,干燥后测得质量为27.2g.下列有关推断正确的是( )
| A、参加反应HNO3物质的量为0.9mol |
| B、参加反应的金属质量为11.9g |
| C、HNO3物质的量浓度为3mol/L |
| D、NaOH物质的量浓度为6mol/L |
当下列各组物质的总物质的量保持不变时,组内各成分以任意比例混合充分燃烧,消耗O2的量和生成的CO2的量都不变的是( )
| A、乙烯 乙醛 |
| B、乙炔 乙二醇 |
| C、甲烷 甲醇 |
| D、甲烷 乙醇 |
如图所示,将锌片和铜片通过导线相连,置于稀硫酸中.下列说法正确的是( )
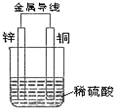

| A、铜片上有气泡逸出 |
| B、溶液的SO42-浓度逐渐减小 |
| C、电子由铜片经导线流向锌片 |
| D、该装置能将电能转化为化学能 |