��Ŀ����
��ͼ��ʾ�ķ�Ӧ��ϵ�У����ֲ��ﱻ��ȥ����֪2mol��ɫ�����ĩX���ȷֽ⣬�ָ����������ɰ�ɫ����A����ɫҺ��B����ɫ����C��1mol��X��E��G����ɫ��Ӧ��Ϊ��ɫ��
 ��ش��������⣺
��ش��������⣺
��1��д���������ʵĻ�ѧʽ��X�� ��C�� ��
��2��д��Na2O2��C��Ӧ�Ļ�ѧ����ʽ ���÷�Ӧ���������� ����ԭ���� ��
��3��д��A+C+B��X�Ļ�ѧ����ʽΪ ��
��4�����ں�0.5molA����Һ�еμ���2mol/L������300ml������������ڱ�������Ϊ L��
 ��ش��������⣺
��ش��������⣺��1��д���������ʵĻ�ѧʽ��X��
��2��д��Na2O2��C��Ӧ�Ļ�ѧ����ʽ
��3��д��A+C+B��X�Ļ�ѧ����ʽΪ
��4�����ں�0.5molA����Һ�еμ���2mol/L������300ml������������ڱ�������Ϊ
���㣺������ƶ�,�Ƶ���Ҫ������
ר�⣺�ƶ���,������Ҫ�Ľ������仯����
������X��E��G����ɫ��Ӧ��Ϊ��ɫ��������NaԪ�أ�
X�ֽ�������ɫҺ��B����BΪH2O��B
E
G����֪EΪNaOH��GΪNaAlO2��
��ɫ����C��Na2O2��Ӧ���ɰ�ɫ����A��CΪCO2��A��Na2CO3��2mol��ɫ�����ĩX���ȷֽ⣬���ɰ�ɫ����1molNa2CO3��1molH2O��1molCO2������Ԫ���غ��֪��XΪNaHCO3����NaOH��Ӧ����Na2CO3��Na2CO3
CO2��CO2+NaAlO2��D��DΪAl��OH��3������ת����ϵ��NaHCO3+F��CO2��F������������εȣ���϶�Ӧ���ʵ������Լ���ĿҪ������⣮
X�ֽ�������ɫҺ��B����BΪH2O��B
| Na2O2 |
| Al |
��ɫ����C��Na2O2��Ӧ���ɰ�ɫ����A��CΪCO2��A��Na2CO3��2mol��ɫ�����ĩX���ȷֽ⣬���ɰ�ɫ����1molNa2CO3��1molH2O��1molCO2������Ԫ���غ��֪��XΪNaHCO3����NaOH��Ӧ����Na2CO3��Na2CO3
| �������� |
���
�⣺X��E��G����ɫ��Ӧ��Ϊ��ɫ��������NaԪ�أ�
X�ֽ�������ɫҺ��B����BΪH2O��B
E
G����֪EΪNaOH��GΪNaAlO2��
��ɫ����C��Na2O2��Ӧ���ɰ�ɫ����A��CΪCO2��A��Na2CO3��2mol��ɫ�����ĩX���ȷֽ⣬���ɰ�ɫ����1molNa2CO3��1molH2O��1molCO2������Ԫ���غ��֪��XΪNaHCO3����NaOH��Ӧ����Na2CO3��Na2CO3
CO2��CO2+NaAlO2��D��DΪAl��OH��3������ת����ϵ��NaHCO3+F��CO2��F������������εȣ�
��1�������Ϸ�����֪XΪNaHCO3��CΪCO2���ʴ�Ϊ��NaHCO3��CO2��
��2��CΪCO2����Na2O2��ӦΪ2Na2O2+2CO2=2Na2CO3+O2����Ӧ��OԪ�ػ��ϼ���-1�۽���Ϊ-2�ۣ���-1����Ϊ0�ۣ�Na2O2�������������ǻ�ԭ����
�ʴ�Ϊ��2Na2O2+2CO2=2Na2CO3+O2��Na2O2��Na2O2��
��3��A��Na2CO3��BΪH2O��CΪCO2����Ӧ������NaHCO3������ʽΪNa2CO3+CO2+H2O=2 NaHCO3��
�ʴ�Ϊ��Na2CO3+CO2+H2O=2 NaHCO3��
��4��n��HCl��=2mol/L��0.3L=0.6mol��
�Ⱥ���Na2CO3+HCl=NaHCO3+NaCl��
0.5mol 0.5mol
NaHCO3+HCl=H2O+CO2+NaCl��
0.1mol 0.1mol 0.1mol
�ɷ���ʽ��֪����0.1molCO2�����Ϊ22.4L��
�ʴ�Ϊ��2.24��
X�ֽ�������ɫҺ��B����BΪH2O��B
| Na2O2 |
| Al |
��ɫ����C��Na2O2��Ӧ���ɰ�ɫ����A��CΪCO2��A��Na2CO3��2mol��ɫ�����ĩX���ȷֽ⣬���ɰ�ɫ����1molNa2CO3��1molH2O��1molCO2������Ԫ���غ��֪��XΪNaHCO3����NaOH��Ӧ����Na2CO3��Na2CO3
| �������� |
��1�������Ϸ�����֪XΪNaHCO3��CΪCO2���ʴ�Ϊ��NaHCO3��CO2��
��2��CΪCO2����Na2O2��ӦΪ2Na2O2+2CO2=2Na2CO3+O2����Ӧ��OԪ�ػ��ϼ���-1�۽���Ϊ-2�ۣ���-1����Ϊ0�ۣ�Na2O2�������������ǻ�ԭ����
�ʴ�Ϊ��2Na2O2+2CO2=2Na2CO3+O2��Na2O2��Na2O2��
��3��A��Na2CO3��BΪH2O��CΪCO2����Ӧ������NaHCO3������ʽΪNa2CO3+CO2+H2O=2 NaHCO3��
�ʴ�Ϊ��Na2CO3+CO2+H2O=2 NaHCO3��
��4��n��HCl��=2mol/L��0.3L=0.6mol��
�Ⱥ���Na2CO3+HCl=NaHCO3+NaCl��
0.5mol 0.5mol
NaHCO3+HCl=H2O+CO2+NaCl��
0.1mol 0.1mol 0.1mol
�ɷ���ʽ��֪����0.1molCO2�����Ϊ22.4L��
�ʴ�Ϊ��2.24��
����������������ͼ�����ʽ����Na��Al��Ԫ�ص��ʼ���������ת����ϵ�����û�ѧ������д��������ԭ��Ӧ����ȣ��Ѷ��еȣ���ɫҺ��B��X��E��G����ɫ��Ӧ��Ϊ��ɫ���ǽ���ͻ�ƿڣ��������C��Na2O2��Ӧ����˳�Ʒ������Ʒ������ƶϣ���ѧ������������������ϸߵ�Ҫ��

��ϰ��ϵ�д�
�����Ŀ
��һ�ܱ������У��õ����ʵ�����A��B�������·�Ӧ��A������+2B������?2C��������Ӧ��5min ʱ��A��ת����Ϊ0.4�����ʱ����������ʵ���n��A����n��B����n��C��Ӧ����Ĺ�ϵ�ǣ�������
| A��n��A��=n��C�� |
| B��n��B��=n��C�� |
| C��n��A��+n��B��=n��C�� |
| D��n��B��+n��C��=n��A�� |
������ʵ���У�������������ȷ���ǣ�������
| A����������ƿ�з��뼸�����Ƭ����ֹҺ�屩�� |
| B�����¶ȼ�ˮ�������������ƿ֧�ܿڸ��� |
| C����ˮ���������¿��룬�Ͽڳ� |
| D��������ƿ���õ�ʯ��������ֱ�Ӽ��� |
�����л������������ȷ���ǣ�������
| A��HCHO ��ȩ |
| B��C6H5OH ���� |
| C��CH3Cl 1-�ȼ��� |
D��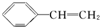 ����ϩ ����ϩ |
���бȽ��У���ȷ���ǣ�������
| A�����ʵ���Ũ����ȵĴ�����Һ������������Һ�������ϣ�c��Na+��+c��H+��=c��CH3COO-��+c��OH-��+c��CH3COOH�� |
| B��0.2mol/L NH4NO3��0.1 mol/L NaOH��Һ�������Ϻ�c��NH4+����c��NO3-����c��Na+����c��OH-����c��H+�� |
| C�������£�ͬŨ�ȵ�һԪ��HA��HB���룬����ͬŨ�ȵ�NaA��Һ��NaB��Һ��pH�� |
| D��ͬŨ�ȵ�������Һ����NH4Al��SO4��2����NH4Cl����NH3?H2O����CH3COONH4������c��NH4+���ɴ�С��˳���ǣ��٣��ڣ��ܣ��� |
 ij��ʳƷ�����ϱ�ǩ��ͼ��ʾ��
ij��ʳƷ�����ϱ�ǩ��ͼ��ʾ��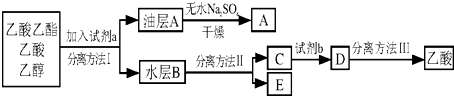
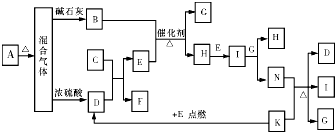 ��ͼ�е�B��K�ֱ�����йط�Ӧ��һ�ַ�Ӧ������������A��C��F��K�ǹ��壻E�dz��������嵥�ʣ�I�Ǻ���ɫ����̬�������̬����A���������Ⱥ����ɵ�����������ͨ����ʯ��ֻʣ������B����ͨ��Ũ������ֻʣ������D�������ʼ��ת����ϵ��ͼ��ʾ����ش��������⣺
��ͼ�е�B��K�ֱ�����йط�Ӧ��һ�ַ�Ӧ������������A��C��F��K�ǹ��壻E�dz��������嵥�ʣ�I�Ǻ���ɫ����̬�������̬����A���������Ⱥ����ɵ�����������ͨ����ʯ��ֻʣ������B����ͨ��Ũ������ֻʣ������D�������ʼ��ת����ϵ��ͼ��ʾ����ش��������⣺