题目内容
下列实验中,不会产生沉淀的是( )
| A、CO2通入水玻璃中 |
| B、CO2 通入偏铝酸钠溶液中 |
| C、SO2通入氯化钡溶液中 |
| D、SO2通入氢氧化钙溶液中 |
考点:钠的重要化合物,二氧化硫的化学性质
专题:元素及其化合物
分析:因碳酸酸性比硅酸、氢氧化铝强,则二氧化碳可与硅酸钠、偏铝酸钠溶液反应生成沉淀,亚硫酸酸性比盐酸弱,二氧化硫可与氢氧化钙反应生成亚硫酸钙沉淀,以此解答.
解答:
解:A.CO2通入水玻璃中,可生成硅酸沉淀,故A不选;
B.CO2 通入偏铝酸钠溶液中,可生成氢氧化铝沉淀,故B不选;
C.亚硫酸酸性比盐酸弱,SO2通入氯化钡溶液中,不反应,没有沉淀生成,故C选;
D.SO2通入氢氧化钙溶液中,可生成亚硫酸钙沉淀,故D不选.
故选C.
B.CO2 通入偏铝酸钠溶液中,可生成氢氧化铝沉淀,故B不选;
C.亚硫酸酸性比盐酸弱,SO2通入氯化钡溶液中,不反应,没有沉淀生成,故C选;
D.SO2通入氢氧化钙溶液中,可生成亚硫酸钙沉淀,故D不选.
故选C.
点评:本题综合考查元素化合物知识,为高考常见题型,侧重于学生的分析能力和基础知识的综合理解和运用的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
常温下,下列各组离子在指定溶液中可能大量共存的是( )
| A、含[Ag(NH3)2]+的溶液:K+、OH-、NH3?H2O、Cl- | ||||
B、使甲基橙试液变黄色的溶液:Na+、Cu2+、HCO-3、N
| ||||
C、与Al能够产生H2的溶液:Mg2+、K+、S
| ||||
| D、含Fe(OH)3胶体的溶液:Na+、Fe2+、I-、SCN- |
 如图是a、b两种固体物质的溶解度曲线.下列说法中正确的是( )
如图是a、b两种固体物质的溶解度曲线.下列说法中正确的是( )| A、a物质的溶解度受温度变化的影响较小,b物质的溶解度受温度变化的影响较大 |
| B、t℃时,等质量的a、b饱和溶液中含有相同质量的溶质 |
| C、当温度大于t℃时,a溶液一定比b溶液浓 |
| D、a中含有少量b时,用冷却热饱和溶液的方法提纯a |
家用消毒液发生器是化学知识在日常生活中的“创新”应用.该发生器利用常见的精盐和自来水为反应物.通电时,发生器内电解槽里的极板上产生大量水泡.切断电源后所得的消毒液有强烈的杀菌能力,且对人体无害.溶液中发生的主要的反应为
2NaCl+2H2O=2NaOH+H2+Cl2 2NaOH+Cl2=NaCl+NaClO+H2O则所得消毒液的有效成分是( )
2NaCl+2H2O=2NaOH+H2+Cl2 2NaOH+Cl2=NaCl+NaClO+H2O则所得消毒液的有效成分是( )
| A、NaCl |
| B、Cl2 |
| C、NaClO |
| D、HClO |
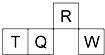 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A、含T的盐溶液一定显酸性 |
| B、最高价氧化物对应水化物的酸性:Q<W |
| C、原子半径:T>Q>R |
| D、最简单气态氢化物的热稳定性:R>Q |
相同温度下,在体积相同的两个密闭容器内充入等质量的CO2和SO2气体,则下列说法中正确的是( )
| A、CO2和SO2的物质的量相同 |
| B、CO2和SO2的密度比为11:16 |
| C、CO2和SO2的压强比为16:11 |
| D、CO2和SO2中所含氧原子的个数比为1:1 |
下列说法正确的是( )
| A、摩尔是用于描述微观粒子的物理量 |
| B、0.012kg12C所含的原子数精确值是6.02×1023 |
| C、1mol H2的体积为22.4L |
| D、1molH2SO4的质量是98g |
下列离子方程式正确的是( )
| A、饱和碳酸钠溶液中通入过量的CO2:CO32-+H2O+CO2=2HCO3- |
| B、氯气跟水反应:Cl2+H2O=2H++Cl-+ClO- |
| C、过氧化钠投入水中:Na2O2+H2O=2Na++2OH-+O2↑ |
| D、氯化铝溶液中加入过量氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
下列离子方程式与所述事实不相符的是( )
| A、苯酚钠溶液中通入少量CO2:C6H5O-+CO2+H2O→C6H5OH+HCO3- | ||
| B、在碳酸氢钠溶液中加入过量的氢氧化钡溶液:Ba2++OH-+HCO3-═BaCO3↓+H2O | ||
C、用新制的氢氧化铜悬浊液检验乙醛中的醛基:CH3CHO+2Cu(OH)2+OH-
| ||
| D、向Ca(ClO)2溶液中通入过量SO2:Ca2++2ClO-+SO2+H2O=CaSO4↓+2H++Cl-+HClO |