题目内容
8.下列关于装置图的叙述中,不正确的是( )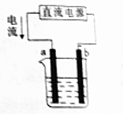
| A. | a为阳极 | |
| B. | 和b相连的电源一极发生还原反应 | |
| C. | 用该装置在铁上镀铜时,b为铁块 | |
| D. | 用该装置点解精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液 |
分析 A、电解池中电流由电源的正极流向电解池的阳极,所以a是电解池的阳极;
B、电解池中电流由电源的正极流向电解池的阳极,则b是电解池的阴极,和b相连的电源一极是负极;
C、镀件是电解池的阴极;
D、精炼铜时粗铜是阳极,纯铜是阴极.
解答 解:A、电解池中电流由电源的正极流向电解池的阳极,所以a是电解池的阳极,故A正确;
B、电解池中电流由电源的正极流向电解池的阳极,则b是电解池的阴极,和b相连的电源一极是负极,发生氧化反应,故B错误;
C、镀件是电解池的阴极,所以铁上镀铜时,b为铁块,故C正确;
D、精炼铜时粗铜是阳极,纯铜是阴极,电解质含有镀层金属阳离子的盐溶液,所以则a极为粗铜,电解质溶液为CuSO4溶液,故D正确;
故选B.
点评 本题考查了原电池和电解池原理,明确电极反应的自发性确定正负极,再结合阴阳极上发生的电极反应来分析解答,比较容易.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
18.下列有关化学用语正确的是( )
| A. | NH4Cl的电子式: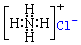 | B. | 中子数为18的氯原子:${\;}_{17}^{35}$Cl | ||
| C. | 碳酸的电离:H2CO3?2H++CO32- | D. | 次氯酸的结构式:H-Cl-O |
13.0.2mol•dm-3甲酸溶液中有3.2%的甲酸电离,它的电离常数是( )
| A. | 9.6×10-3 | B. | 4.8×10-5 | C. | 1.25×10-6 | D. | 2.0×10-4 |
20.下列实验方案设计正确的是( )
| A. | 分解高锰酸钾制氧气后,残留在试管内壁上的黑色物质可用稀盐酸洗涤 | |
| B. | 将CuCl2溶液在蒸发皿中加热蒸干,得到无水CuCl2固体 | |
| C. | 失去标签的硝酸银溶液、稀盐酸、氢氧化钠溶液、氯化铝溶液,可以用碳酸铵溶液鉴别 | |
| D. | 检验从火星上带回来的红色物体是否是Fe2O3的操作步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液 |
17.某温度时,Ag2SO4在水中的沉淀溶解曲线如图所示.该温度下,下列说法正确的是( )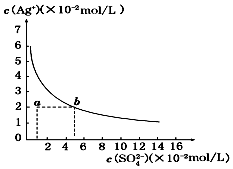

| A. | 含有大量SO42-的溶液中肯定不存在Ag+ | |
| B. | 0.02 mol/L的AgNO3溶液与0.2 mol/L的Na2SO4溶液等体积混合不会生成沉淀 | |
| C. | Ag2SO4的溶度积常数(Ksp)为1×10-3 | |
| D. | a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到b点 |
18.能正确表示下列反应的离子方程式是( )
| A. | Cl2通入NaOH溶液:Cl2+OH-=Cl-+ClO-+H2O | |
| B. | NaHCO3溶液中加入稀HCl:CO32-+2H+=CO2↑+H2O | |
| C. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O=[Al(OH)4]-+4NH4+ | |
| D. | Cu溶于稀HNO3:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O |