题目内容
下列叙述中,可以用来判断金属性强弱的是( )
| A、一个金属原子失去电子的多少 |
| B、1mol金属跟酸反应放出氢气的多少 |
| C、金属最高价氧化物对应水化物的碱性强弱 |
| D、金属氢化物形成的难易 |
考点:金属在元素周期表中的位置及其性质递变的规律
专题:元素周期律与元素周期表专题
分析:A、金属性强弱与失去电子的难易程度有关,与失去电子数目多少没有关系;
B、物质的量相同,生成的氢气越多,金属失去的电子越多,金属性强弱与失去电子的难易程度有关,与失去电子数目多少没有关系;
C、金属元素的最高价氧化物对应的水化物的碱性越强,则失电子能力越强;
D、金属一般不容易形成金属氢化物.
B、物质的量相同,生成的氢气越多,金属失去的电子越多,金属性强弱与失去电子的难易程度有关,与失去电子数目多少没有关系;
C、金属元素的最高价氧化物对应的水化物的碱性越强,则失电子能力越强;
D、金属一般不容易形成金属氢化物.
解答:
解:A、金属性强弱与失去电子的难易程度有关,与失去电子数目多少没有关系,如Al、Mg与盐酸反应,Al失去的电子多,但金属性Mg强于Al,1mol金属单质失电子的多少由原子结构决定,与失电子能力强弱无关,故A错误;
B、物质的量相同,生成的氢气越多,说明金属失去的电子越多,金属性强弱与失去电子的难易程度有关,与失去电子数目多少没有关系,故B错误;
C、金属元素的最高价氧化物对应的水化物的碱性越强,则失电子能力越强,可以通过金属元素的最高价氧化物对应的水化物的碱性强弱判断金属性强弱,故C正确;
D、金属一般不容易形成金属氢化物,不能根据金属是否易形成金属氢化物来判断金属性强弱,故D错误;
故选C.
B、物质的量相同,生成的氢气越多,说明金属失去的电子越多,金属性强弱与失去电子的难易程度有关,与失去电子数目多少没有关系,故B错误;
C、金属元素的最高价氧化物对应的水化物的碱性越强,则失电子能力越强,可以通过金属元素的最高价氧化物对应的水化物的碱性强弱判断金属性强弱,故C正确;
D、金属一般不容易形成金属氢化物,不能根据金属是否易形成金属氢化物来判断金属性强弱,故D错误;
故选C.
点评:本题考查学生元素性质和元素周期表的递变规律知识,注意把握金属性强弱的判断方法,难度并不大.

练习册系列答案
相关题目
氯碱工业的一种节能新工艺,将电解池与燃料电池相组合,相关物料的传输与转化关系如图所示(电极未标出):
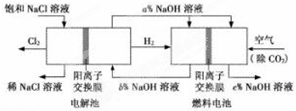
下列说法正确的是( )

下列说法正确的是( )
| A、电解池的阴极反应式为H++2e-=H2↑ |
| B、通入空气的电极为负极 |
| C、电解池中产生2mol Cl2,理论上燃料电池中消耗0.5 mol O2 |
| D、a、b、c的大小关系为:a>b=c |
反应2X(g)?2Y(g)+2Z(g)△H>0达到平衡时,要使正反应速率降低,X的浓度增大,应采取的措施是( )
| A、加压 | B、减压 |
| C、减小Z的浓度 | D、降温 |
下列关于液氯、新制氯水叙述中不正确的是( )
| A、都具有酸性 |
| B、都能使湿润的有色布条褪色 |
| C、都含Cl2 |
| D、液氯是纯净物,而新制氯水是混合物 |
电解质在人体内的作用是非常广泛和十分重要的.当电解质的平衡被破坏时,人体就要出现一系列不适症状,甚至危及生命.为维持人体内电解质平衡,在大量出汗后应及时补充的离子是( )
| A、Mg2+ |
| B、Ca2+ |
| C、Na+ |
| D、Fe3+ |
下了各组中的两物质作用时,反应条件或者是反应用量的改变,对生成物没有影响的是( )
| A、Na2O2和CO2 |
| B、Na和 O2 |
| C、NaOH 和CO2 |
| D、C和O2 |
相同质量的H2 和O2它们之间的关系是( )
| A、所含原子的物质的量之比为1:1 |
| B、所含分子的物质的量之比为1:1 |
| C、所含原子的物质的量之比为16:1 |
| D、所含分子的物质的量之比为1:16 |
普罗加比是目前临床上应用的主要抗癫痫药物之一,它可由A经多步反应合成. 
下列说法正确的是( )

下列说法正确的是( )
| A、物质A分子中在同一平面上的原子最多为12个 |
| B、1 mol中间体最多能与7 mol H2发生加成反应 |
| C、普罗加比可与Na2CO3溶液发生反应 |
| D、物质A、中间体和普罗加比都易溶于水 |