题目内容
能正确表示下列化学变化的离子方程式是( )
| A、钠和冷水反应:Na+2H2O=Na++2OH-+H2↑ |
| B、氯气与溴化钠溶液反应:Cl2+2Br-=Br2+2Cl- |
| C、氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2Cl- |
| D、三氯化铁溶液与氢氧化钠溶液反应:FeCl3+3OH-=Fe(OH)3↓+3Cl- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.根据电荷守恒判断,该离子方程式两边电荷不守恒;
B.氯气氧化性大于溴单质,氯气能够将溴离子氧化成溴单质;
C.根据电荷守恒判断,该离子方程式两边电荷不守恒;
D.氯化铁为可溶性的盐,离子方程式中氯化铁应该写成离子形式.
B.氯气氧化性大于溴单质,氯气能够将溴离子氧化成溴单质;
C.根据电荷守恒判断,该离子方程式两边电荷不守恒;
D.氯化铁为可溶性的盐,离子方程式中氯化铁应该写成离子形式.
解答:
解:A.钠和冷水反应生成氢氧化钠和氢气,离子方程式中必须满足电荷守恒,正确的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,故A错误;
B.氯气与溴化钠溶液反应生成溴和氯离子,反应的离子方程式为:Cl2+2Br-=Br2+2Cl-,故B正确;
C.氯化亚铁溶液中通入氯气,该离子方程式两边电荷不守恒,正确的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,故C错误;
D.三氯化铁溶液与氢氧化钠溶液反应生成氢氧化铁沉淀,氯化铁应该写成离子形式,正确的离子方程式为:Fe3++3OH-=Fe(OH)3↓,故D错误;
故选B.
B.氯气与溴化钠溶液反应生成溴和氯离子,反应的离子方程式为:Cl2+2Br-=Br2+2Cl-,故B正确;
C.氯化亚铁溶液中通入氯气,该离子方程式两边电荷不守恒,正确的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,故C错误;
D.三氯化铁溶液与氢氧化钠溶液反应生成氢氧化铁沉淀,氯化铁应该写成离子形式,正确的离子方程式为:Fe3++3OH-=Fe(OH)3↓,故D错误;
故选B.
点评:本题考查了离子方程式的书写判断,题目难度中等,注意掌握离子方程式的书写原则,明确常见难溶物、弱电解质等需要保留化学式的物质;注意电荷守恒、质量守恒的应用.

练习册系列答案
相关题目
下列措施一定能增大化学反应速率的是( )
| A、增大反应物浓度 |
| B、降低温度 |
| C、减小反应物的浓度 |
| D、使用催化剂 |
某研究性学习小组的同学做了一个趣味实验:将一只鸡蛋放入食醋中,过一会发现蛋壳表面附有气泡,第二天蛋壳就变软了.你认为鸡蛋壳与食醋发生反应的离子方程式正确的是( )
| A、CO32-+2H+→H2O+CO2↑ |
| B、CaCO3+2H+→Ca2++H2O+CO2↑ |
| C、CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑ |
| D、CO32-+2CH3COOH→2CH3COO-+H2O+CO2↑ |
互为同素异形体的一组物质是( )
A、
| ||||
| B、O2和O3 | ||||
| C、CH≡CH和CH2=CH2 | ||||
D、CH3CH2CH2CH3和 |
下列各装置中,能够成原电池的是( )
A、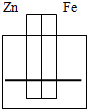 乙醇 |
B、 稀硫酸 |
C、 稀硫酸 |
D、 稀硫酸 稀硫酸 |
 如图为铁铜水果(呈酸性)电池的示意图,下列说法正确的是( )
如图为铁铜水果(呈酸性)电池的示意图,下列说法正确的是( )| A、铁是负极 |
| B、铜极附近呈蓝色 |
| C、铜极上发生氧化反应 |
| D、电子由铜经导线流向铁 |
 【化学反应原理(选修4)】
【化学反应原理(选修4)】