题目内容
下列说法正确的是( )
| A、等物质的量浓度的 ①NH4HSO4、②NH4HCO3、③NH4Cl溶液中,c(NH4+)的大小关系:①>②>③ |
| B、pH相同的CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液:c(CH3COO-)>c(CO32-)>c(C6H5O-) |
| C、常温下,取0.3mol/L HY溶液与0.3mol/L NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=9,则由水电离出的c(OH-)=10-9 mol/L |
| D、c(NH4+)=c(Cl-)的NH4Cl溶液一定呈中性 |
考点:离子浓度大小的比较,盐类水解的应用,酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题,盐类的水解专题
分析:A.氢离子抑制铵根离子水解、碳酸氢根离子促进铵根离子水解,铵根离子水解程度越大,相同物质的量浓度的 铵盐溶液中铵根离子浓度越小;
B.根据盐对应的酸的酸辛强弱比较水解程度;
C.取0.3mol/L HY溶液与0.3mol/L NaOH溶液等体积混合(忽略混合后溶液体积的变化),二者恰好反应生成NaY,测得混合溶液的pH=9,说明NaY是强碱弱酸盐,溶液中水电离出的c(OH-)=10-3 mol/L;
D.任何电解质溶液中都存在电荷守恒,根据电荷守恒判断.
B.根据盐对应的酸的酸辛强弱比较水解程度;
C.取0.3mol/L HY溶液与0.3mol/L NaOH溶液等体积混合(忽略混合后溶液体积的变化),二者恰好反应生成NaY,测得混合溶液的pH=9,说明NaY是强碱弱酸盐,溶液中水电离出的c(OH-)=10-3 mol/L;
D.任何电解质溶液中都存在电荷守恒,根据电荷守恒判断.
解答:
解:A.氢离子抑制铵根离子水解、碳酸氢根离子促进铵根离子水解,铵根离子水解程度越大,相同物质的量浓度的 铵盐溶液中铵根离子浓度越小,所以等物质的量浓度的 ①NH4HSO4、②NH4HCO3、③NH4Cl溶液中,c(NH4+)的大小关系:①>③>②,故A错误;
B.已知酸性:CH3COOH>C6H5OH>HCO3-,酸性越弱,对应的盐类水解程度越大,则pH相同的CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液:c(CH3COO-)>c(C6H5O-)>c(CO32-),故B错误;
C.取0.3mol/L HY溶液与0.3mol/L NaOH溶液等体积混合(忽略混合后溶液体积的变化),二者恰好反应生成NaY,测得混合溶液的pH=9,说明NaY是强碱弱酸盐,溶液中水电离出的c(OH-)为溶液中氢氧根离子浓度=10-3 mol/L,故C错误;
D.如果NH4Cl溶液中c(NH4+)=c(Cl-),任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(H+)=c(OH-),所以溶液呈中性,故D正确;
故选D.
B.已知酸性:CH3COOH>C6H5OH>HCO3-,酸性越弱,对应的盐类水解程度越大,则pH相同的CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液:c(CH3COO-)>c(C6H5O-)>c(CO32-),故B错误;
C.取0.3mol/L HY溶液与0.3mol/L NaOH溶液等体积混合(忽略混合后溶液体积的变化),二者恰好反应生成NaY,测得混合溶液的pH=9,说明NaY是强碱弱酸盐,溶液中水电离出的c(OH-)为溶液中氢氧根离子浓度=10-3 mol/L,故C错误;
D.如果NH4Cl溶液中c(NH4+)=c(Cl-),任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(H+)=c(OH-),所以溶液呈中性,故D正确;
故选D.
点评:本题考查了离子浓度大小比较,根据盐的性质及盐类水解程度确定离子浓度大小,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
关于丙烯醛(CH2=CH-CHO)的下列叙述中,正确的是( )
| A、在丙烯醛分子中,仅含有一种官能团 |
| B、丙烯醛不能使溴水褪色,但能使酸性高锰酸钾溶液褪色 |
C、丙烯醛能发生缩聚反应,生成高聚物 |
| D、等物质的量的丙烯醛和乙烷完全燃烧,消耗等物质的量的氧气 |
下列过程能肯定是放热反应的是( )
| A、燃烧 | B、分解 | C、凝华 | D、溶解 |
有关如图所示化合物的说法不正确的是( )


| A、既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应 |
| B、既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体 |
| C、既可以催化加氢,又可以使酸性KmnO4溶液褪色 |
| D、1mol该化合物最多可以与3mol NaOH反应 |
如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
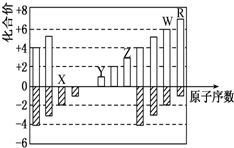

| A、原子半径:Z>Y>X |
| B、气态氢化物的稳定性:R>W |
| C、WX3和水反应形成的化合物是离子化合物 |
| D、2mol Z单质与足量Y的最高氧化物对应的水化物的溶液反应,有2mol H2O被还原 |
氢有H、D、T三种同位素,氯有35Cl、37Cl两种同位素,则形成的氯化氢分子的种类有( )
| A、2 | B、5 | C、6 | D、9 |
 石蜡油(主要是含17个碳原子以上的液态烷烃混合物)分解实验按照右图进行:
石蜡油(主要是含17个碳原子以上的液态烷烃混合物)分解实验按照右图进行: