题目内容
19.下列说法不正确的是( )| A. | 硅可用于制造电脑芯片 | B. | 浓H2SO4可用做干燥剂 | ||
| C. | 碳酸氢钠可用于食品的发酵 | D. | 少量金属钠保存在酒精中 |
分析 A.Si为半导体材料;
B.浓硫酸具有吸水性;
C.碳酸氢钠与发酵酸反应生成气体;
D.Na与酒精反应生成氢气.
解答 解:A.Si为半导体材料,可用于制造电脑芯片,故A正确;
B.浓硫酸具有吸水性,则可用做干燥剂,故B正确;
C.碳酸氢钠与发酵酸反应生成气体,则可用于食品的发酵,故C正确;
D.Na与酒精反应生成氢气,则Na应保存在煤油中,隔绝空气,故D错误;
故选D.
点评 本题考查物质的性质及应用,为高频考点,把握元物质的性质、发生的反应、性质与用途为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
10.下列关于有机化合物的说法错误的是( )
| A. | 2,2-二甲基丙烷也称新戊烷 | |
| B. | 由乙烯生成乙醇属于加成反应 | |
| C. | 分子式为C5H11Cl的有机物共有8种(不含立体异构) | |
| D. | 所有的糖类、油脂、蛋白质都可以发生水解反应 |
14.下列属于碱的是( )
| A. | Na2SO4 | B. | NaOH | C. | H2SO4 | D. | CO2 |
4.一定温度下,在2L的密闭容器中发生反应:xA(g)+B(g)?2C(g)△H<0,A、C的物质的量随时间变化的关系如表所示.下列有关说法正确的是( )
| 时间/min | n(A)mol | n(C)mol |
| 0 | 0.3 | 0 |
| 1 | 0.15 | 0.15 |
| 2 | 0.1 | 0.2 |
| 3 | 0.1 | 0.2 |
| A. | x=1 | |
| B. | 反应开始2min内,用B表示的反应速率为0.05mol•L-l•min -1 | |
| C. | 反应进行到lmin时,反应体系达到化学平衡状态 | |
| D. | A的正反应速率等于C的逆反应速率时,反应体系达到化学平衡状态 |
11.下列说法不正确的是( )
| A. | 氯化钠熔化时离子键被破坏 | |
| B. | 二氧化硅融化和干冰气化所破坏的作用力不相同 | |
| C. | H2SO4、CCl4、NH3均属于共价化合物 | |
| D. | HBr比HCl的热稳定性差说明HBr的分子间作用力比HCl弱 |
16.在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是( )
| A. | CH3OH(l)+O2(g)═CO2(g)+2H2O(l);△H=+725.8kJ/mol | |
| B. | 2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l);△H=-1452kJ/mol | |
| C. | 2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l);△H=-725.8kJ/mol | |
| D. | 2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l);△H=+1452kJ/mol |
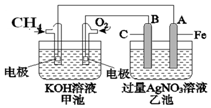 如图是一个化学过程的示意图.请回答下列问题:
如图是一个化学过程的示意图.请回答下列问题: