题目内容
草酸是二元弱酸,草酸氢钾溶液呈酸性。在0.1mol·L-1 KHC2O4溶液中,下列关系正确的是
A.c(K+)+c(H+) = c(HC2O4-)+c(OH-)+c(C2O42-)
B.c(HC2O4-)+c(C2O42-) = 0.1 mol·L-1
C.c(C2O42-) < c(H2C2O4)
D.c(K+) = c(H2C2O4)+c(HC2O4-)+c(C2O42-)
D
【解析】
试题分析:草酸氢钾溶液呈酸性,说明HC2O4-的电离作用大于其水解作用。A.根据电荷守恒可得c(K+)+c(H+) = c(HC2O4-)+c(OH-)+2c(C2O42-),A错误。B.根据物料守恒可得c(HC2O4-)+c(C2O42-)+ c(H2C2O4)= 0.1 mol/L。B错误。C.在草酸氢钾溶液中存在电离平衡:HC2O4- C2O42-+ H+;电离使溶液显酸性。同时也存在水解平衡:HC2O4-+H2O
C2O42-+ H+;电离使溶液显酸性。同时也存在水解平衡:HC2O4-+H2O H2C2O4+ OH-。水解是溶液显碱性。由于电离作用大于水解作用。所以c(C2O42-) > c(H2C2O4),C错误。D.根据物料守恒,c(K+) = c(H2C2O4)+c(HC2O4-)+c(C2O42-),D正确,选D。
H2C2O4+ OH-。水解是溶液显碱性。由于电离作用大于水解作用。所以c(C2O42-) > c(H2C2O4),C错误。D.根据物料守恒,c(K+) = c(H2C2O4)+c(HC2O4-)+c(C2O42-),D正确,选D。
考点:考查溶液中离子浓度的大小比较的知识。

 53随堂测系列答案
53随堂测系列答案关于下列装置说法正确的是
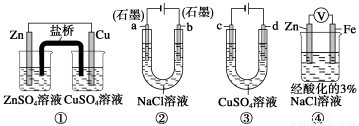
A.装置①中,盐桥中的K+移向CuSO4溶液装置
B.②工作一段时间后,a极附近溶液的pH减小
C.用装置③精炼铜时,c极为粗铜
D.装置④中电子由Zn流向Fe,装置中有Fe2+生成
(8分)现有失去标签的氯化钙、硝酸银、盐酸、碳酸钠四种无色溶液,为了确定四种溶液各是什么,将它们随意编上A、B、C、D后, 产生的现象如下表所示。根据实验现象回答出A、B、C、D溶液中溶质的化学式:
A ;B ;C ;D ;
实验顺序 | 实验内容 | 实验现象 |
① | A+B | 没有现象发生 |
② | B+D | 有气体放出 |
③ | B+C | 有沉淀生成 |
④ | A+D | 有沉淀生成 |