题目内容
16.某同学设计如图装置,探究氯碱工业原理,下列说法正确的是( )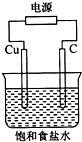
| A. | 石墨电极与直流电源负极相连 | |
| B. | 铜电极的反应式为:2H++2e-═H2↑ | |
| C. | 氢氧化钠在石墨电极附近产生,Na+向石墨电极迁移 | |
| D. | 用湿润KI淀粉试剂在铜电极附近检验气体,试纸变蓝色 |
分析 氯碱工业原理:阳极上氯离子失电子生成氯气,阴极上氢离子得电子生成氢气,根据电极反应结合图象分析.
解答 解:氯碱工业原理:阳极上氯离子失电子生成氯气,阴极上氢离子得电子生成氢气,由图可知Cu为阴极(若铜为阳极,则铜失电子,氯离子不反应),C为阳极,
A、石墨为阳极,与直流电源的正极相连,故A错误;
B、Cu为阴极,阴极上氢离子得电子生成氢气,铜电极的反应式为:2H++2e-═H2↑,故B正确;
C、Cu为阴极,阴极上氢离子得电子生成氢气,同时生成氢氧化钠,电解池中阳离子向阴极移动,Na+向Cu电极移动,故C错误;
D、Cu为阴极,阴极上氢离子得电子生成氢气,没有氯气生成,所以用湿润KI淀粉试剂在铜电极附近检验气体,试纸不变蓝色,故D错误.
故选B.
点评 本题考查了电解原理的应用,侧重于电极的判断和电极方程式的书写的考查,题目难度不大,注意把握氯碱工业的原理.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.有关NaHCO3和Na2CO3的性质,下列叙述错误的是( )
| A. | 等质量的两种盐与足量盐酸反应,在相同条件下Na2CO3产生的CO2的体积小 | |
| B. | 等物质的量的两种盐与同浓度盐酸完全反应,所消耗盐酸的体积Na2CO3是NaHCO3两倍 | |
| C. | 将石灰水加入NaHCO3溶液中不产生沉淀,加入Na2CO3溶液中产生白色沉淀 | |
| D. | 等物质的量浓度的两种溶液,Na2CO3溶液的pH大于NaHCO3溶液的pH |
11.不能用胶体知识理解的现象是( )
| A. | 阳光通过门缝有光亮通路 | |
| B. | 一支钢笔使两种不同牌号的墨水,容易出现堵塞 | |
| C. | 向氯化铁溶液中加 NaOH溶液,会出现红褐色沉淀 | |
| D. | 在河水与海水的交界处,易形成三角洲 |
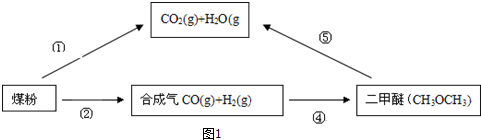
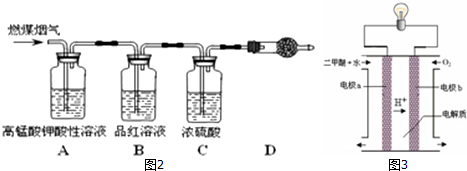
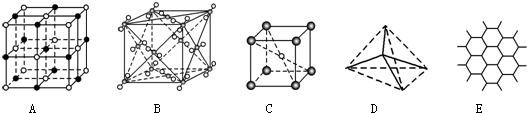
 .
.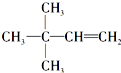 等.
等. .
.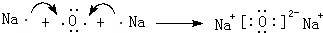 .
.