题目内容
9.实验室用软锰矿(MnO2)与浓盐酸加热制氯气,下列说法正确的是( )| A. | 盛浓盐酸的分液漏斗可用长颈漏斗代替 | |
| B. | 可在集气瓶口放一张湿润的淀粉碘化钾试纸,观察氯气是否收集满 | |
| C. | 用饱和食盐水吸收尾气 | |
| D. | 为了便于学生观察氯气的制备实验,可在讲台上直接做氯气的制备实验 |
分析 A.若分液漏斗用长颈漏斗代替,无法控制加入浓盐酸的体积;
B.氯气具有强的氧化性,能够氧化碘离子生成单质碘;
C.氯气在饱和食盐水中溶解度不大;
D.氯气有毒,容易造成空气污染.
解答 解:A.实验室制取氯气时,为了便于控制加入浓盐酸的量,需要用分液漏斗盛放浓盐酸,不能用长颈漏斗代替,故A错误;
B.氯气具有强的氧化性,能够氧化碘离子生成单质碘,碘与淀粉变蓝,故B正确;
C.氯气在饱和食盐水中溶解度不大,不能用饱和食盐水吸收过量氯气,故C错误;
D.氯气有毒,容易造成空气污染,制备氯气应在通风橱中进行,故D错误;
故选B.
点评 本题考查了化学实验方案的评价,题目难度不大,明确实验室中氯气的制备原理及装置特点为解答关键,B为易错点,注意饱和食盐水可除去氯气中的氯化氢,不能收集氯气,试题侧重基础知识的考查,有利于提高学生的分析能力及化学实验能力.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
20.铝可以制成多种建筑型材,铝在空气中能够稳定存在的原因是( )
| A. | 铝的密度小 | B. | 铝表面能形成致密的氧化膜 | ||
| C. | 常温下铝不能与氧气反应 | D. | 铝的化学性质不活泼 |
4.某无色透明的溶液,在pH=0和pH=14的条件下都能大量共存的是( )
| A. | Na+ K+ SO42- AlO2- | B. | Ca2+ Na+ SO42- Cl- | ||
| C. | Na+ K+ SO42- NO3- | D. | K+ Na+ MnO4- SO42- |
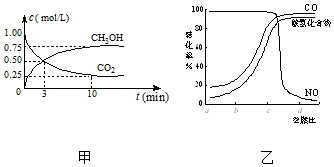 CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径.
CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径.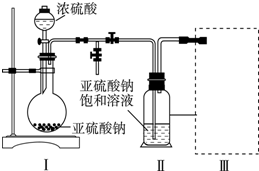
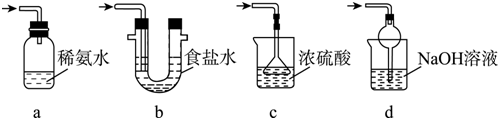
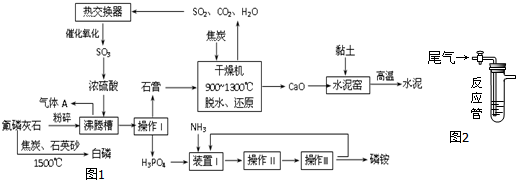
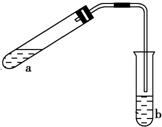 可用如图所示的装置制取少量乙酸乙酯(酒精灯等在图中均已略去).请填空:
可用如图所示的装置制取少量乙酸乙酯(酒精灯等在图中均已略去).请填空: