题目内容
3.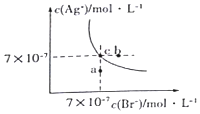 在t°C时,AgBr在水中的沉淀溶解平衡曲线如图所示.又知t°C时AgCl的Ksp=4×10-10,下列说法不正确的是( )
在t°C时,AgBr在水中的沉淀溶解平衡曲线如图所示.又知t°C时AgCl的Ksp=4×10-10,下列说法不正确的是( )| A. | 图中a点对应的是AgBr的不饱和溶液 | |
| B. | 在t°C时,AgBr的Ksp为 4.9×10-13 | |
| C. | 在AgBr饱和溶液中加入NaBr固体,可使溶液由c点到b点 | |
| D. | 在t°C时,AgCl(s)+Br-(aq)?AgBr(s)+C1-(aq)的平衡常数K≈816 |
分析 A.a点在曲线的下方,c(Br-)c(Ag+)<Ksp(AgBr);
B.t°C时,c点Ksp=c(Br-)c(Ag+);
C.在AgBr饱和溶液中加入NaBr固体,c(Br-)增大,溶解平衡逆向移动,c(Ag+)减小;
D.在t°C时,AgCl(s)+Br-(aq)?AgBr(s)+C1-(aq)的平衡常数K=$\frac{c(C{l}^{-})}{c(B{r}^{-})}$=$\frac{Ksp(AgCl)}{Ksp(AgBr)}$.
解答 解:A.a点在曲线的下方,c(Br-)c(Ag+)<Ksp(AgBr),对应的是AgBr的不饱和溶液,故A正确;
B.t°C时,c点Ksp=c(Br-)c(Ag+)=7×10-7×7×10-7=4.9×10-13,故B正确;
C.在AgBr饱和溶液中加入NaBr固体,c(Br-)增大,溶解平衡逆向移动,c(Ag+)减小,而由c点到b点c(Ag+)不变,则不能使溶液由c点到b点,故C错误;
D.在t°C时,AgCl(s)+Br-(aq)?AgBr(s)+C1-(aq)的平衡常数K=$\frac{c(C{l}^{-})}{c(B{r}^{-})}$=$\frac{Ksp(AgCl)}{Ksp(AgBr)}$=$\frac{4×1{0}^{-10}}{4.9×1{0}^{-13}}$≈816,故D正确;
故选C.
点评 本题考查难溶电解质的溶解平衡,为高频考点,把握图在离子浓度变化与Ksp的关系、Qc与Ksp的关系、K与Ksp的关系为解答的关键,侧重分析与应用能力的考查,注意选项C为易错点,题目难度不大.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
13.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 25℃时pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| B. | 标准状况下,22.4L的CCl4中含有CCl4分子数目为NA | |
| C. | 25℃时,1L 1mol•L-1的NaClO溶液中含有ClO-的数目为NA | |
| D. | 6.4gCu与一定浓度的HNO3完全反应得到混合气体,转移的电子数目为0.2NA |
14.在c(NaOH)=2c(NaAlO2)的溶液中滴加稀HCl,下列离子方程式正确的是( )
| A. | OH-+AlO2-+2H+=Al(OH)3 | B. | OH-+AlO2-+5H+=Al3++3H2O | ||
| C. | 2OH-+AlO2-+3H+=Al(OH)3+H2O | D. | OH-+2AlO2-+3H++H2O=2Al(OH)3 |
11.关于胶体.下列说法正确的是( )
| A. | 胶体就是直径为10-9m~10-7m的微粒 | |
| B. | 实验室制备Fe(OH)3胶体的方法是将饱和FeCl3溶液滴入NaOH溶液并加热 | |
| C. | 电解Fe(OH)3胶体,阴极附近红褐色加深,是因为胶体带正电,向阴极移动 | |
| D. | 可以用丁达尔效应来区别胶体和溶液 |
8.水是一种宝贵的自然资源,水体污染危害很大,我们要爱护水资源.下列现象与水体污染无关的是( )
| A. | 水俣病 | B. | 赤潮 | C. | 水华 | D. | 潮汐 |
15.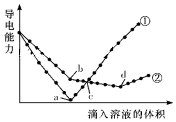 在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析正确的是( )
在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析正确的是( )
 在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析正确的是( )
在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析正确的是( )| A. | ②代表滴加H2SO4溶液的变化曲线 | |
| B. | b点溶液中大量存在的离子是SO42-、Na+、OH- | |
| C. | a、d两点对应的溶液均显中性 | |
| D. | c点两溶液中含有相同量的OH- |
12.已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是元素周期表中原子半径最小的元素,Y元素形成的化合物种类最多,Z是短周期中金属性最强的元素,W的单质是一种黄色晶体或粉末.下列说法不正确的是( )
| A. | 离子半径:Z>W | |
| B. | 对应的氢化物的热稳定性:R>W | |
| C. | X与Z、W与Z均以原子个数比1:1形成的化合物中化学键类型不完全相同 | |
| D. | R的最高价氧化物的水化物与NaHYO3溶液反应有气泡生成,证明非金属性:R>Y |
13.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 在标准状况下,1mol O2 与1mol 纯碱的体积相同 | |
| B. | 常温常压下,18g H2O所含的氧原子的数目为NA | |
| C. | 0.1mol Zn与含0.1mol HCl的盐酸充分反应,转移的电子数目为0.2NA | |
| D. | 1L 水溶解58.5g NaCl 所形成的溶液的物质的量浓度是0.1mol•L-1 |